题目内容
19.下列解释事实的方程式正确的是( )| A. | 钢铁生锈,负极反应式为Fe-3e-═Fe3+ | |
| B. | 用石墨做电极电解硫酸铜溶液,有Cu和O2析出:2Cu2++OH-$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+2H2O | |
| C. | Na2CO3溶液滴加酚酞,溶液变红:CO32-+2H2O?H2CO3+2O2↑ | |
| D. | 酸性高锰酸钾溶液中加入草酸钠,溶液褪色:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O |
分析 A.Fe失去电子生成亚铁离子;
B.石墨做电极电解硫酸铜溶液,水中的氢氧根离子放电;
C.水解为可逆反应,且碳酸根离子水解以第一步为主;
D.发生氧化还原反应,遵循电子、电荷守恒.
解答 解:A.钢铁生锈,负极反应式为Fe-2e-═Fe2+,故A错误;
B.用石墨做电极电解硫酸铜溶液,有Cu和O2析出,离子反应为2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+,故B错误;
C.Na2CO3溶液滴加酚酞,溶液变红,发生水解离子反应为CO32-+H2O?HCO3-+OH-,故C错误;
D.酸性高锰酸钾溶液中加入草酸钠,溶液褪色的离子反应为2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重电解、水解、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 3.55gCl2通入足量水中充分反应,转移电子数为0.05NA | |
| B. | 18gNH4+含有质子数为10NA | |
| C. | 13.8gNO2与足量水反应时,转移电子的数目为0.2NA | |
| D. | 标准状况下,相同体积的SO3、HCl、NO含有的分子数相同 |
7.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 11.2 L NH3中所含的原子数为2NA | |
| B. | 2.4g金属镁变为Mg2+时失去的电子数为0.1 NA | |
| C. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA个 | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA个 |
14.实验室用足量镁粉与一定量的盐酸反应来制取氢气,由于盐酸浓度太大,反应不易控制.为减慢反应速率,同时又不影响生成H2的总量,可向盐酸中加入的物质有( )
①NaOH固体 ②NH4Cl固体 ③CH3COONa溶液 ④K2SO4固体 ⑤加入适量水.
①NaOH固体 ②NH4Cl固体 ③CH3COONa溶液 ④K2SO4固体 ⑤加入适量水.
| A. | ③⑤ | B. | ②③ | C. | ②④ | D. | ①④ |
4.某无色溶液能与镁反应放出氢气,此溶液中可能大量共存的离子组是( )
| A. | NH4+、Mg2+、SO42-、Cl- | B. | Fe3+、K+、Cl-、NO3- | ||
| C. | K+、Ba2+、NO3-、SO42- | D. | Na+、NH4+、Cl-、CO32- |
11.表中是食用碘盐包装上的部分说明,下列说法正确的是( )
| 配料 | 精盐、碘酸钾(KIO3)、抗结剂 |
| 碘含量 | 35±15mg/kg |
| 储存方法 | 密封、避光、防潮 |
| 食用方法 | 烹饪时,待食品熟后加入碘盐 |
| A. | 高温会导致碘的损失 | B. | 碘酸钾可氧化氯化钠 | ||
| C. | 可用淀粉检验碘盐中的碘酸钾 | D. | 该碘盐中碘含量是指碘酸钾的含量 |
8.用接触法制5t98%的浓硫酸,在理论上需要FeS270%(杂质不含碳元素)的硫铁矿为( )
| A. | 86t | B. | 8.6t | C. | 4.3t | D. | 43t |
 在实验室里,第一位同学取一小块金属钠做与水反应的实验.试完成下列问题:
在实验室里,第一位同学取一小块金属钠做与水反应的实验.试完成下列问题: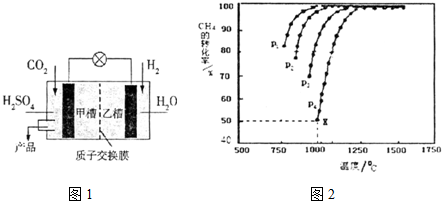 第21届联合国气候大会于2015年11月30日在巴黎召开,会议的主题是减 少温室气体排放量.
第21届联合国气候大会于2015年11月30日在巴黎召开,会议的主题是减 少温室气体排放量.