题目内容
3.某温度下,将C12通人NaOH溶液中,反应得到NaCI、NaClO、NaClO3的混合液,经测定CIO-与ClO3-的浓度之比为1:2,则Cl2与NaOH溶液反应时被还原的氯元素和被氧化的氯元素的物质的量之比为( )| A. | 21:5 | B. | 11:3 | C. | 1:4 | D. | 4:1 |
分析 Cl2和NaOH溶液中,反应得到NaCI、NaClO、NaClO3的混合液,Cl2既是氧化剂又是还原剂,如果混合溶液中c(ClO-):c(ClO3-)=1:2,根据转移电子守恒计算NaCl物质的量,被还原的Cl元素和被氧化的Cl元素就是生成NaCl的氯元素和生成ClO-、ClO3-的Cl元素,据此分析解答.
解答 解:Cl2和NaOH溶液中,反应得到NaCI、NaClO、NaClO3的混合液,Cl2既是氧化剂又是还原剂,如果混合溶液中c(ClO-):c(ClO3-)=1:2,设c(ClO-)、c(ClO3-)的物质的量浓度分别是1mol/L、2mol/L,根据转移电子守恒计算c(NaCl)=$\frac{1+2×5}{1}$=11mol/L,所以被还原的Cl元素和被氧化的Cl元素就是生成NaCl的氯元素和生成ClO-、ClO3-的Cl元素,溶液体积相等,所以被还原的Cl元素和被氧化的Cl元素的物质的量之比为11:(1+2)=11:3,
故选:B.
点评 本题考查氧化还原反应的计算,明确转移电子相等是解本题关键,侧重考查学生对基本概念、基本理论的理解和运用,知道常见元素化合价,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列仪器不能用于加热的是( )
| A. | 量筒 | B. | 试管 | C. | 蒸发皿 | D. | 烧瓶 |
14.下列离子能大量共存的是( )
| A. | 含有大量Ba(NO3 )2的溶液中:Mg2+、NH4+、SO42-、Cl- | |
| B. | 无色透明的溶液中:Cu2+、K+、SO42-、NO3- | |
| C. | 在碱性溶液中:Na+、K+、SO42-、CO32- | |
| D. | 在酸性的溶液中:Na+、K+、CO32-、NO3- |
11.某化妆品的组分Z具有美白功效,原从杨树中提取,现可用如下反应制备:
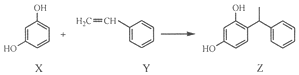
下列叙述错误的是( )

下列叙述错误的是( )
| A. | X和Z均能与FeCl3溶液反应显紫色 | |
| B. | X和Z均能与NaHCO3溶液反应放出CO2 | |
| C. | Y既能发生取代反应,也能发生加成反应 | |
| D. | Y可作加聚反应单体,X可作缩聚反应单体 |
18.表中对于相关物质的分类全部正确的一组是( )
| 编号 | 纯净物 | 混合物 | 碱性氧化物 | 非电解质 |
| A | 液氯 | 漂白粉 | Al2O3 | CO |
| B | 纯碱 | 浓硫酸 | CaO | 乙醇 |
| C | 碱石灰 | 王水 | K2O | Cl2 |
| D | 胆矾 | 水玻璃 | Na2O2 | SO2 |
| A. | A | B. | B | C. | C | D. | D |
15.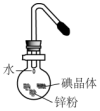 将碘研碎后与锌粉混合于蒸发皿中,然后滴加少量水,可观察到紫红色蒸气产生,此实验被称为“滴水生烟”.关于该实验的下列说法中错误的是( )
将碘研碎后与锌粉混合于蒸发皿中,然后滴加少量水,可观察到紫红色蒸气产生,此实验被称为“滴水生烟”.关于该实验的下列说法中错误的是( )
 将碘研碎后与锌粉混合于蒸发皿中,然后滴加少量水,可观察到紫红色蒸气产生,此实验被称为“滴水生烟”.关于该实验的下列说法中错误的是( )
将碘研碎后与锌粉混合于蒸发皿中,然后滴加少量水,可观察到紫红色蒸气产生,此实验被称为“滴水生烟”.关于该实验的下列说法中错误的是( )| A. | Zn与I2的反应是放热反应 | B. | 水在该反应中作催化剂 | ||
| C. | 生成的碘化锌为紫红色 | D. | 紫红色的蒸气是碘升华所致 |
16.有一真空瓶质量为 m1,该瓶充入空气后质量为 m2.在相同状况下,若改为充入某气体 A 时,总质量为 m3.则 A 的相对分子质量是( )
| A. | 29$\frac{{m}_{2}}{{m}_{1}}$ | B. | 29$\frac{{m}_{3}}{{m}_{1}}$ | ||
| C. | 29$\frac{{m}_{3}-{m}_{1}}{{m}_{2}-{m}_{1}}$ | D. | 29$\frac{{m}_{2}-{m}_{1}}{{m}_{3}-{m}_{1}}$ |