题目内容
12.下列离子方程式中,错误的是( )| A. | 少量SO2通入足量NaOH溶液中:SO2+2OH-═SO32-+H2O | |
| B. | 将氨通入稀硫酸中:NH3+H+═NH4+ | |
| C. | 在NaOH溶液中滴入NH4Cl溶液并加热:NH4+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3+H2O | |
| D. | 向Ba(OH)2溶液中加入稀H2SO4恰好完全反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
分析 A.二氧化硫少量,反应生成亚硫酸钠和水;
B.氨气与硫酸反应生成硫酸铵;
C.在NaOH溶液中滴入NH4Cl溶液并加热反应生成氨气、氯化钠和水;
D.离子个数配比不符合物质结构.
解答 解:A.少量SO2通入足量NaOH溶液中,离子方程式:SO2+2OH-═SO32-+H2O,故A正确;
B.将氨通入稀硫酸中,离子方程式:NH3+H+═NH4+,故B正确;
C.在NaOH溶液中滴入NH4Cl溶液并加热,离子方程式:NH4+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3+H2O,故C正确;
D.向Ba(OH)2溶液中加入稀H2SO4恰好完全反应,离子方程式:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故D错误;
故选:D.
点评 本题考查离子反应方程式的书写,明确发生的化学反应即可解答,侧重反应的实质及离子反应中保留化学式的物质的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是( )
| A. | SO2、SiO2、CO、P2O5都是非金属元素形成的氧化物,均为酸性氧化物 | |
| B. | HClO、H2SO4(浓)、HNO3均具有氧化性,都是氧化性酸 | |
| C. | BaCl2、Ca(OH)2、HNO3、HT 均为化合物 | |
| D. | HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质 |
20.aR3-和bMn+的核外电子数相等,则a值等于( )
| A. | b+n+3 | B. | b+n-3 | C. | b-n+3 | D. | b-n-3 |
7.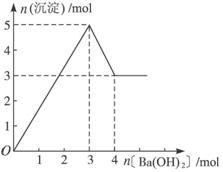 如图表示在某溶液中滴加Ba(OH) 2溶液时,沉淀的物质的量随Ba(OH) 2的物质的量的变化关系.该溶液的成分可能是( )
如图表示在某溶液中滴加Ba(OH) 2溶液时,沉淀的物质的量随Ba(OH) 2的物质的量的变化关系.该溶液的成分可能是( )
 如图表示在某溶液中滴加Ba(OH) 2溶液时,沉淀的物质的量随Ba(OH) 2的物质的量的变化关系.该溶液的成分可能是( )
如图表示在某溶液中滴加Ba(OH) 2溶液时,沉淀的物质的量随Ba(OH) 2的物质的量的变化关系.该溶液的成分可能是( )| A. | MgSO 4 | B. | Al 2(SO 4) 3 | C. | Fe 2(SO 4) 3 | D. | NaAlO 2 |
17.下列试剂的保存方法不正确的是( )
| A. | NaOH溶液保存在配有玻璃塞的细口瓶中 | |
| B. | 金属钠通常密封保存在煤油中 | |
| C. | 氯水通常保存在棕色细口瓶并置于阴凉处 | |
| D. | 氢氟酸保存在塑料试剂瓶中 |
1. 三草酸合铁酸钾晶体(K3[Fe(C2O4)3]•xH2O)是一种光敏材料,110℃时失去全部结晶水.某实验小组为测定该晶体中铁的含量,做了如下实验,完成下列填空:
三草酸合铁酸钾晶体(K3[Fe(C2O4)3]•xH2O)是一种光敏材料,110℃时失去全部结晶水.某实验小组为测定该晶体中铁的含量,做了如下实验,完成下列填空:
步骤一:称取5.0g三草酸合铁酸钾晶体,配制成250mL溶液.
步骤二:取所配溶液25.00mL于锥形瓶中,加H2SO4酸化,滴加KMnO4溶液,发生反应
2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O(Mn2+视为无色).向反应后的溶液中加入锌粉,
加热至黄色刚好消失,过滤并洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性.
步骤三:用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,滴定中MnO4-被还原成Mn2+.消耗KMnO4溶液体积如表所示:
(1)步骤一所用仪器已有托盘天平(带砝码)、玻璃棒、烧杯、药匙,还缺少的仪器250mL容量瓶、胶头滴管.
(2)加入锌粉的目的是将Fe3+恰好还原成Fe2+,使Fe2+在步骤三中与KMnO4发生氧化还原反应.
(3)写出步骤三中发生反应的离子方程式5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O.
(4)实验测得该晶体中铁元素的质量分数为11.2%.在步骤二中,若滴加的KMnO4溶液的量不够,则测得铁的含量偏高.(选填“偏低”、“偏高”或“不变”)
 三草酸合铁酸钾晶体(K3[Fe(C2O4)3]•xH2O)是一种光敏材料,110℃时失去全部结晶水.某实验小组为测定该晶体中铁的含量,做了如下实验,完成下列填空:
三草酸合铁酸钾晶体(K3[Fe(C2O4)3]•xH2O)是一种光敏材料,110℃时失去全部结晶水.某实验小组为测定该晶体中铁的含量,做了如下实验,完成下列填空:步骤一:称取5.0g三草酸合铁酸钾晶体,配制成250mL溶液.
步骤二:取所配溶液25.00mL于锥形瓶中,加H2SO4酸化,滴加KMnO4溶液,发生反应
2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O(Mn2+视为无色).向反应后的溶液中加入锌粉,
加热至黄色刚好消失,过滤并洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性.
步骤三:用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,滴定中MnO4-被还原成Mn2+.消耗KMnO4溶液体积如表所示:
| 滴定次数 | 滴定起始读数(mL) | 滴定终点读数(mL) |
| 第一次 | 1.08 | 见右图 |
| 第二次 | 2.02 | 24.52 |
| 第三次 | 1.00 | 20.98 |
(2)加入锌粉的目的是将Fe3+恰好还原成Fe2+,使Fe2+在步骤三中与KMnO4发生氧化还原反应.
(3)写出步骤三中发生反应的离子方程式5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O.
(4)实验测得该晶体中铁元素的质量分数为11.2%.在步骤二中,若滴加的KMnO4溶液的量不够,则测得铁的含量偏高.(选填“偏低”、“偏高”或“不变”)

