题目内容
下列措施不能加快锌与稀H2SO4反应速率的是( )
| A、加入少量CuSO4固体 |
| B、将Zn粒改为Zn粉 |
| C、增大压强 |
| D、加热 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:加快该反应速率,可增大浓度、升高温度、增大固体表面积,以此解答该题.
解答:
解:A、Zn与硫酸铜反应生成铜,形成锌铜原电池,加快反应速率,故A不选;
B、Zn粒该为Zn粉,增大了接触面积,反应速率加快,故B不选;
C、在溶液中进行的反应,压强的改变对反应速率无影响,故C选;
D、加热,增大了活化分子的百分数,反应速率加快,故D不选;
故选C.
B、Zn粒该为Zn粉,增大了接触面积,反应速率加快,故B不选;
C、在溶液中进行的反应,压强的改变对反应速率无影响,故C选;
D、加热,增大了活化分子的百分数,反应速率加快,故D不选;
故选C.
点评:本题考查反应速率的影响因素,为高考高频考点,注意把握影响反应速率的因素,难度不大,学习中注意相关基础知识的积累.

练习册系列答案
相关题目
除去下列括号内杂质的试剂或方法错误的是( )
| A、HNO3溶液(H2SO4),适量BaCl2溶液,过滤 |
| B、Fe2+(Fe3+),还原铁粉,过滤 |
| C、Cl2(HCl),饱和食盐水,洗气 |
| D、CO2(SO2),饱和NaHCO3溶液,洗气 |
在室温下,下列叙述正确的是( )
| A、两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2 | ||
| B、Na2CO3溶液加水稀释后,恢复至原温度,pH和KW均减小 | ||
| C、pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等 | ||
D、向0.1 mol?L-1的氨水中加入少量硫酸铵固体,则溶液中
|
在200mL含Mg2+、Al3+、NH4+、H+、Cl-离子的溶液中,逐滴加人4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mo1)的关系如图所示.下列叙述正确的是( )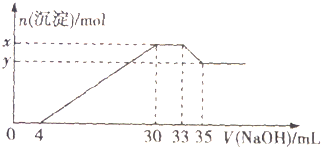

| A、原溶液中n(Mg2+):n(A13+)=10:1 |
| B、原溶液中c(H+)=0.8mol/L |
| C、x与y的差值为0.08 |
| D、原溶液中c(C1-)=0.66mol/L |
在呼吸面具和潜水艇里,过滤空气的最佳物质是( )
| A、NaOH |
| B、Na2O2 |
| C、Na |
| D、Al |
如图是某硫酸试剂瓶标签上的部分文字.据此,下列说法正确的是( )


| A、该硫酸的物质的量浓度为9.2mol?L-1 |
| B、1 mol Zn与足量的该硫酸反应生成2g氢气 |
| C、该硫酸与等体积水混合所得溶液的物质的量浓度等于9.2mol?L-1 |
| D、向50 mL该硫酸溶液中加入足量的铜片,加热充分反应后,被还原的硫酸的物质的量小于0.46 mol |
 1000℃时,硫酸钠可与氢气发生反应:Na2SO4(s)+4H2(g)?Na2S(s)+4H2O(g).请回答下列问题:
1000℃时,硫酸钠可与氢气发生反应:Na2SO4(s)+4H2(g)?Na2S(s)+4H2O(g).请回答下列问题: