题目内容
1.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可使用的试剂是( )| A. | NaOH | B. | KSCN | C. | KMnO4 | D. | 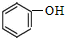 |
分析 亚铁离子具有还原性,可与氯水、高锰酸钾等氧化剂反应,以此解答该题.
解答 解:A.加入氢氧化钠,因含有铁离子,可生成红褐色沉淀,不能检验是否含有亚铁离子,故A错误;
B.亚铁离子与KSCN不反应,不能鉴别,只能鉴别铁离子,故B错误;
C.亚铁离子具有还原性,可与高锰酸钾等发生氧化还原反应,高锰酸钾溶液褪色,可鉴别,故C正确;
D.亚铁离子与苯酚不反应,不能鉴别,只能鉴别铁离子,故D错误.
故选C.
点评 本题考查物质的检验,为高频考点,题目难度不大,本题注意亚铁离子与铁离子性质的区别,检验时必须有明显不同的现象.

练习册系列答案
相关题目
11.用惰性电极电解下列溶液,一段时间后停止电解,向溶液中加入一定质量的另一种物质(括号内),能使溶液完全恢复的是( )
| A. | CuCl2(CuO) | B. | NaOH(NaOH) | C. | CuSO4(CuO) | D. | NaCl(盐酸) |
12.下列物质不是常见的室内污染物是( )
| A. | 甲苯 | B. | 甲醛 | C. | NO2 | D. | 氡 |
16.化学与生产、生活息息相关,下列叙述错误的是( )
| A. | 铁表而镀铜可以增强其抗腐蚀性 | |
| B. | 用高温催化氧化法去除烃类废气(CxHy):CxHy+(x+$\frac{y}{4}$)O2$→_{高温}^{催化剂}$xCO2+$\frac{y}{2}$H2O | |
| C. | 大量燃烧化石燃料是造成雾霾天气的一种重要因素 | |
| D. | 废旧电池中含有的重金属离子对水和土壤会造成污染,因而不能随意丢弃 |
6.设NA表示阿伏加德罗常数的值,下列有关NA的叙述中正确的是( )
| A. | 惰性电极电解饱和食盐水,若电路中通过NA个电子,则阳极产生气体11.2L | |
| B. | 在反应KIO3+6HI=KI+3I2+3H2O中,每生成3mol I2转移的电子数为6NA | |
| C. | 1 mol C12发生化学反应,转移的电子数必为2NA | |
| D. | 标准状况下,4.0 g CH4中含有共价键的数目为NA |
13.砖瓦是用含铁等元素的黏土隔绝空气烧制而成的.当烧窑作业临近结束时,若用淋水的办法来降低温度,窑内处于还原性气氛,则砖呈青色,称青砖.若用捅开窑顶自然冷却的办法,则砖呈红色,称红砖.由此判断砖块中的成分,错误的是( )
| A. | 砖块中的主要成分是硅酸盐 | |
| B. | 青砖中的铁元素主要以氢氧化亚铁的形式存在 | |
| C. | 红砖中的铁元素主要以氧化铁的形式存在 | |
| D. | 青砖中的铁元素主要以氧化亚铁的形式存在 |
10.化学与工农业生产有密切的联系.下列说法中正确的是( )
| A. | 分子式为(C6H10O5)n的淀粉和纤维素互为同分异构体 | |
| B. | 淀粉、蛋白质、脂肪都是营养物质,都属于高分子化合物 | |
| C. | 在蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,虽再加水,也不溶解 | |
| D. | 北京奥运吉祥物“福娃”的材质是PVC(聚氯乙烯),其单体的结构是CH2=CHCl |
19. 用O2将HCl转化为Cl2,可提高效益,减少污染,
用O2将HCl转化为Cl2,可提高效益,减少污染,
(1)传统上该转化通过如图所示的催化剂循环实现,其中,反应①为:2HCl(g)+CuO(s)?H2O(g)+CuCl2(g)△H1反应②生成1molCl2(g)的反应热为△H2,则总反应的热化学方程式为2HCl(g)+$\frac{1}{2}$O2(g)?H2O(g)+Cl2(g),△H=(△H1+△H2)kJ/mol,(反应热用△H1和△H2表示).
(2)新型RuO2催化剂对上述HCl转化为Cl2的总反应具有更好的催化活性,
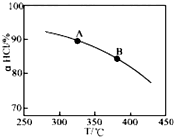
①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的aHCl-T曲线如图,则总反应的△H<0,(填“>”、“﹦”或“<”);A、B两点的平衡常数K(A)与K(B)中较大的是K(A).
②在上述实验中若压缩体积使压强增大,画出相应aHCl-T(HCl的转化率与温度的关系)曲线的示意图,并简要说明理由: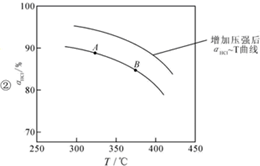 增大压强,平衡右移,ɑHCl增大,相同温度下,HCl的平衡转化率比之前实验的大.
增大压强,平衡右移,ɑHCl增大,相同温度下,HCl的平衡转化率比之前实验的大.
③下列措施中有利于提高aHCl的有BD.
A、增大n(HCl) B、增大n(O2) C、使用更好的催化剂 D、移去H2O
(3)一定条件下测得反应过程中n(Cl2)的数据如下:
计算2.0~6.0min内以HCl的物质的量变化表示的反应速率(以mol•min-1为单位,写出计算过程).
(4)Cl2用途广泛,写出用Cl2制备漂白粉的化学方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
 用O2将HCl转化为Cl2,可提高效益,减少污染,
用O2将HCl转化为Cl2,可提高效益,减少污染,(1)传统上该转化通过如图所示的催化剂循环实现,其中,反应①为:2HCl(g)+CuO(s)?H2O(g)+CuCl2(g)△H1反应②生成1molCl2(g)的反应热为△H2,则总反应的热化学方程式为2HCl(g)+$\frac{1}{2}$O2(g)?H2O(g)+Cl2(g),△H=(△H1+△H2)kJ/mol,(反应热用△H1和△H2表示).
(2)新型RuO2催化剂对上述HCl转化为Cl2的总反应具有更好的催化活性,
①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的aHCl-T曲线如图,则总反应的△H<0,(填“>”、“﹦”或“<”);A、B两点的平衡常数K(A)与K(B)中较大的是K(A).
②在上述实验中若压缩体积使压强增大,画出相应aHCl-T(HCl的转化率与温度的关系)曲线的示意图,并简要说明理由:
 增大压强,平衡右移,ɑHCl增大,相同温度下,HCl的平衡转化率比之前实验的大.
增大压强,平衡右移,ɑHCl增大,相同温度下,HCl的平衡转化率比之前实验的大.③下列措施中有利于提高aHCl的有BD.
A、增大n(HCl) B、增大n(O2) C、使用更好的催化剂 D、移去H2O
(3)一定条件下测得反应过程中n(Cl2)的数据如下:
| t(min) | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| n(Cl2)/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
(4)Cl2用途广泛,写出用Cl2制备漂白粉的化学方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.