题目内容
15.利用下列反应不能制得括号中纯净物的是 ( )| A. | 等物质的量氯气与乙烷在光照条件下反应(氯乙烷) | |
| B. | 乙烯与水加成(乙醇) | |
| C. | 乙烯与氯气加成(1,2-二氯乙烷) | |
| D. | 乙烯与氢气加成(乙烷) |
分析 A.光照下取代反应为链锁反应;
B.乙烯与水只有一种加成方式;
C.乙烯与氯气只有一种加成方式;
D.乙烯与氢气加成只能生成乙烷.
解答 解:A.光照下取代反应为链锁反应,生成多种卤代烃,不能得到纯净物,故A错误;
B.乙烯与水只有一种加成方式,则只生成乙醇,为纯净物,故B正确;
C.乙烯与氯气只有一种加成方式,只生成1,2-二氯乙烷,为纯净物,故C正确;
D.乙烯与氢气加成只能生成乙烷,生成物为纯净物,故D正确;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应等为解答的关键,侧重分析与应用能力的考查,注意选项A中的反应特点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.常温下,下列有关0.1mol•L-1的NH4Cl溶液的说法正确的是( )
| A. | pH相同的盐酸与氯化铵溶液中,水的电离程度相同 | |
| B. | 溶液加水稀释时,$\frac{c(N{H}_{3}{H}_{2}O)•c({H}^{+})}{c(N{H}_{4}^{+})}$逐渐增大 | |
| C. | 加入少量Mg(OH)2固体,c(NH4+)减小 | |
| D. | 加入等体积0.05mol﹒L-1NaOH溶液时:c(Na+)=c(CI-)>c(NH4+)>c(OH-)>c(H+) |
6.下列互为同位素的是( )
| A. | Na和Na+ | B. | 35Cl和37Cl | ||
| C. | 14N和 14C | D. | ${\;}_{8}^{16}$O2和${\;}_{8}^{18}$O2 |
3.下列叙述错误的是( )
| A. | 乙烯和苯使溴水褪色的原因不同 | |
| B. | 苯和氢气在一定条件下生成环己烷的反应为还原反应 | |
| C. | 硝基苯和乙酸乙酯的制备都发生了取代反应 | |
| D. | 由乙醇制取乙烯发生了氧化反应 |
10.下列说法正确的是( )
| A. | 乙烯与氯气反应生成的产物仍为平面结构 | |
| B. | 甲烷可以与氯气发生反应,因此可以使氯水褪色 | |
| C. | CHCl3只有一种结构,能说明甲烷是正四面体结构 | |
| D. | 邻二氯苯只有一种结构,说明苯环不是单双键交替结构 |
20.在给定条件下,下列选项所示的物质间转化均能实现的是( )
| A. | SiO2$\stackrel{HCl(aq)}{→}$SiCl4$\frac{{H}_{2}}{高温}$Si | |
| B. | MgCO3$\stackrel{HCl(aq)}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg | |
| C. | N2$→_{高温、高压、催化剂}^{H_{2}}$NH${\;}_{{\;}_{3}}$$\stackrel{HCl(aq)}{→}$NH4Cl(aq) | |
| D. | FeS$\stackrel{HCl(aq)}{→}$H2S$→_{煅烧}^{O_{2}}$SO2$→_{点燃}^{氧气}$H2SO4 |
4.相同条件下,下列碱溶液的pH值最大的是( )
| A. | 0.1mol/L氢氧化钠溶液 | B. | 0.1mol/L氢氧化钡溶液 | ||
| C. | 0.1mol/L氢氧化钾溶液 | D. | 0.1mol/L氨水 |
6.草酸是一种重要的试剂.下面是利用草酸探究浓度对反应速率影响的实验.
(1)为证明浓度对反应速率的影响,曾有教科书《化学反应原理》设计了如下实验:取两支试管,各加入4mL0.01mol•L-1的KMnO4酸性溶液,分别向其中加入0.1mol•L-1、0.2mol•L-1 H2C2O4溶液2mL,记录溶液褪色所需时间.
实验中发生反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
预期现象是:
①溶液的颜色由紫色变为无色,
②其中加入0.2mol•L-1H2C2O4的那支试管中的溶液先变色.
然而实验结果并不尽如人意.实验过程颜色复杂,且褪色先缓慢,后逐渐加快;最大的问题是草酸浓度大,反应速率却更慢.
本实验能否作为课堂实验研究浓度对化学反应速率的影响?适宜的条件是怎样的?某校一研究小组对此进行了探究.下面是他们的实验报告的一部分:
表1 试验安排及结果
应用SPSS16.0对正交试验结果进行方差分析,结果如表
表2 各因素水平的数据处理结果
(2)由表2可知,三因素中,C的浓度(选填“A、B或C”,下空同)对反应速率影响显著,而A和B的浓度对反应速率的影响不显著.
(3)由表2可知,当高锰酸钾浓度为0.005mol•L-1、草酸浓度为0.1mol•L-1时,反应最快.即因素A、B的较适宜实验条件得以确定.
根据以上实验结果,该小组同学继续探究硫酸的浓度是怎样影响本反应速率的,测得如下实验结果:
表3 不同硫酸浓度下的褪色时间
(4)根据课堂实验的合适时间,可选溶液的褪色时间约为1分钟和2分钟的两份溶液,即此时硫酸的浓度为18mol•L-1和10mol•L-1,这也有利于观察这两个反应速率的差异.
结论:草酸与酸性高锰酸钾溶液的反应,可作为课堂实验探究浓度对反应速率的影响.
(1)为证明浓度对反应速率的影响,曾有教科书《化学反应原理》设计了如下实验:取两支试管,各加入4mL0.01mol•L-1的KMnO4酸性溶液,分别向其中加入0.1mol•L-1、0.2mol•L-1 H2C2O4溶液2mL,记录溶液褪色所需时间.
实验中发生反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
预期现象是:
①溶液的颜色由紫色变为无色,
②其中加入0.2mol•L-1H2C2O4的那支试管中的溶液先变色.
然而实验结果并不尽如人意.实验过程颜色复杂,且褪色先缓慢,后逐渐加快;最大的问题是草酸浓度大,反应速率却更慢.
本实验能否作为课堂实验研究浓度对化学反应速率的影响?适宜的条件是怎样的?某校一研究小组对此进行了探究.下面是他们的实验报告的一部分:
表1 试验安排及结果
| 实验 编号 | A(KMnO4溶液浓度/mol•L-1) | B(草酸溶液浓度/mol•L-1) | C(硫酸溶液浓度/mol•L-1) | 褪色时间/s |
| 1 | 3 | 3 | 1 | 336 |
| 2 | 1 | 2 | 3 | 82 |
| 3 | 3 | 1 | 3 | 76 |
| 4 | 1 | 3 | 2 | 133 |
| 5 | 2 | 3 | 3 | 102 |
| 6 | 3 | 2 | 2 | 156 |
| 7 | 2 | 2 | 1 | 300 |
| 8 | 2 | 1 | 2 | 115 |
| 9 | 1 | 1 | 1 | 200 |
表2 各因素水平的数据处理结果
| A(KMnO4溶液) | B(草酸溶液) | C(硫酸溶液) | |||||||
| 浓度/mol•L-1 | 0.005 | 0.010 | 0.015 | 0.1 | 0.5 | 0.9 | 6 | 12 | 18 |
| 平均褪色时间/s | 138.3 | 172.3 | 189.3 | 130.3 | 179.3 | 190.3 | 278.7 | 134.7 | 86.7 |
(3)由表2可知,当高锰酸钾浓度为0.005mol•L-1、草酸浓度为0.1mol•L-1时,反应最快.即因素A、B的较适宜实验条件得以确定.
根据以上实验结果,该小组同学继续探究硫酸的浓度是怎样影响本反应速率的,测得如下实验结果:
表3 不同硫酸浓度下的褪色时间
| c(H2SO4)/mol•L-1 | 18 | 16 | 14 | 12 | 10 | 8 | 6 |
| 褪色时间/s | 67 | 83 | 90 | 103 | 129 | 146 | 200 |
结论:草酸与酸性高锰酸钾溶液的反应,可作为课堂实验探究浓度对反应速率的影响.
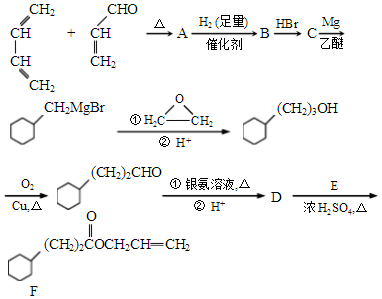
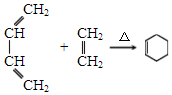
 ,A中所含官能团的名称是醛基、碳碳双键.
,A中所含官能团的名称是醛基、碳碳双键. .
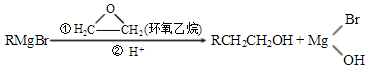
.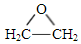 )为原料制备1丁醇,设计合成路线
)为原料制备1丁醇,设计合成路线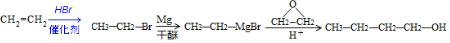 (其它试剂任选).(合成路线常用表示方法为:A $→_{反应条件}^{反应试剂}$ B …$→_{反应条件}^{反应试剂}$目标产物)
(其它试剂任选).(合成路线常用表示方法为:A $→_{反应条件}^{反应试剂}$ B …$→_{反应条件}^{反应试剂}$目标产物)