题目内容
9.在下列事实中,是什么因素影响了化学反应的速率?夏天的食品易发霉,冬天就不易发生该现象.影响因素是温度;
MnO2加入双氧水中反应更剧烈.影响因素是催化剂;
同浓度、同体积的盐酸中放入同样大小的锌粒和镁条,镁条产生气体更快.影响因素是物质本身的性质.
分析 升高温度、增大反应物接触面积、增大反应物浓度、加入催化剂等都增大反应速率,但决定物质反应速率的是物质本身的性质,据此分析解答.
解答 解:夏天温度高,升高温度,增大活化分子百分数,导致反应速率增大,所以夏天的食品易发霉,冬天就不易发生该现象;
二氧化锰作双氧水分解反应的催化剂,增大活化分子百分数,导致反应速率加快;
同浓度、同体积的盐酸中放入同样大小的锌粒和镁条,镁条产生气体更快,因为Mg比Zn活泼,说明决定化学反应速率的是物质本身的性质,
故答案为:温度;催化剂;物质本身的性质.
点评 本题考查化学反应速率影响因素,为高频考点,明确温度、催化剂对化学反应速率影响原理是解本题关键,侧重考查学生分析判断能力,注意:外界因素只是影响因素,决定物质反应速率的是物质本身的性质.

练习册系列答案
相关题目
19.下列物质能使溴的四氯化碳溶液褪色的是( )
| A. | 苯 | B. | 乙烯 | C. | 乙烷 | D. | 乙酸 |
20.下列情况下,气体分子数相同的是( )
| A. | 标准状况下,71gCl2和22.4LHCl | B. | 相同质量的氢气和氮气 | ||
| C. | 在0℃时,1体积的O2和1体积的HCl | D. | 相同体积的CO2和 H2O |
17.稀氨水中存在电离平衡:NH3•H2O?NH4++OH-,若要使平衡正向移动,同时使c(OH-)减小,应加入的物质或采取的措施是( )
①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤通入HCl ⑥加入少量MgSO4固体.
①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤通入HCl ⑥加入少量MgSO4固体.
| A. | ①②⑤ | B. | ①③⑥ | C. | ②④⑤ | D. | ②④⑤⑥ |
4.实验室中以下物质的贮存方法不正确的是( )
| A. | 少量金属钠保存在煤油中 | |
| B. | 试剂瓶中的液溴可用水封存,防止溴挥发 | |
| C. | 保存硫酸亚铁溶液时,要向其中加入少量硫酸和铁粉 | |
| D. | 浓硝酸用带橡胶塞的细口、棕色试剂瓶盛放,并贮存在阴凉处 |
14.将下列各组物质按酸、碱、盐分类顺次排列,其中正确的是( )
| A. | 硫酸 纯碱 孔雀石[Cu2(OH)2CO3] | B. | 硝酸 烧碱 硫酸钡 | ||
| C. | 醋酸 乙醇 碳酸钙 | D. | 盐酸 熟石灰 苛性钠 |
18.向Na[Al(OH)4]溶液中持续通入一种气体,开始时产生沉淀随后沉淀又逐渐溶解,该气体是( )
| A. | NO2 | B. | CO2 | C. | NH3 | D. | CO |
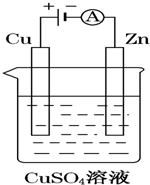 如图是一个电解过程示意图.
如图是一个电解过程示意图.