题目内容
15.关于Na2O和Na2O2的叙述正确的是( )| A. | 都是白色的固体 | B. | 都能和水反应形成强碱溶液 | ||
| C. | 都是碱性氧化物 | D. | 焰色反应的颜色都是紫色 |
分析 A、Na2O是白色固体,Na2O2是淡黄色固体;
B、Na2O与水反应生成氢氧化钠,Na2O2与水反应生成氢氧化钠和氧气;
C、碱性氧化物是指能与酸反应生成盐和水的金属氧化物;
D、钠的焰色反应呈黄色.
解答 解:A、Na2O是白色固体,Na2O2是淡黄色固体,颜色不同,故A错误;
B、Na2O与Na2O2与水反应都能生成氢氧化钠,氢氧化钠是强碱,故B正确;
C、因Na2O2与酸反应生成盐、水和氧气,则Na2O2不属于碱性氧化物,故C错误;
D、Na2O和Na2O2中都含有钠元素,所以焰色反应的颜色都是黄色,故D错误.
故选B.
点评 本题考查钠的氧化物的性质,明确发生的化学反应及相关的概念是解答本题的关键,难度不大.

练习册系列答案
相关题目
5.苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸.反应原理: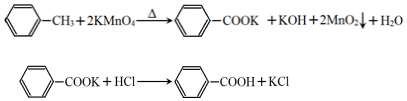
已知:甲苯的熔点为-95℃,沸点为110.6℃,易挥发,密度为0.866g/cm3;
苯甲酸的熔点为122.4℃,在25℃和95℃下在水中溶解度分别为0.344g和6.8g.
Ⅰ.【制备产品】将30.0mL甲苯和25.0mL 1mol/L高锰酸钾溶液在100℃下反应30min,装置如图1所示.
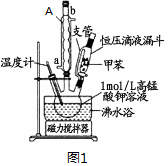
(1)仪器A的名称为冷凝管,A的进水口为a(填“a”或“b”).支管的作用是平衡压强,使甲苯顺利滴入三颈烧瓶.
(2)在本实验中,三颈烧瓶最合适的容积是B(填字母).
A.50mL B.100mL C.250mL D.500mL
Ⅱ.【分离产品】该同学设计如图2流程分离粗产品苯甲酸和回收甲苯.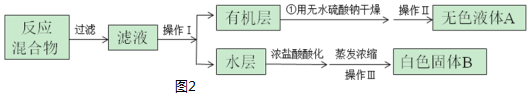
(3)操作Ⅰ的名称是分液;含有杂质的产物经操作Ⅱ进一步提纯得无色液体甲苯,则操作Ⅱ的名称是蒸馏.
Ⅲ.【纯度测定】称取1.220g白色固体,配成100mL甲醇溶液,取25.00mL溶液,用0.1000mol/LKOH标准溶液滴定,重复滴定四次,每次消耗的体积如表所示.
(4)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果偏小(填“偏大”、“偏小”或“不变”).计算样品中苯甲酸纯度为96%.
(5)从白色固体B中得到纯净的苯甲酸的实验方法是:重结晶.

已知:甲苯的熔点为-95℃,沸点为110.6℃,易挥发,密度为0.866g/cm3;
苯甲酸的熔点为122.4℃,在25℃和95℃下在水中溶解度分别为0.344g和6.8g.
Ⅰ.【制备产品】将30.0mL甲苯和25.0mL 1mol/L高锰酸钾溶液在100℃下反应30min,装置如图1所示.

(1)仪器A的名称为冷凝管,A的进水口为a(填“a”或“b”).支管的作用是平衡压强,使甲苯顺利滴入三颈烧瓶.
(2)在本实验中,三颈烧瓶最合适的容积是B(填字母).
A.50mL B.100mL C.250mL D.500mL
Ⅱ.【分离产品】该同学设计如图2流程分离粗产品苯甲酸和回收甲苯.

(3)操作Ⅰ的名称是分液;含有杂质的产物经操作Ⅱ进一步提纯得无色液体甲苯,则操作Ⅱ的名称是蒸馏.
Ⅲ.【纯度测定】称取1.220g白色固体,配成100mL甲醇溶液,取25.00mL溶液,用0.1000mol/LKOH标准溶液滴定,重复滴定四次,每次消耗的体积如表所示.
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
(5)从白色固体B中得到纯净的苯甲酸的实验方法是:重结晶.
10.下列过程中所发生的化学变化属于取代反应的是( )
| A. | 乙炔通入溴水中 | |
| B. | 乙烯通入酸性高锰酸钾溶液中 | |
| C. | 在镍作催化剂的条件下,苯与氢气反应 | |
| D. | 乙烷与氯气光照下发生反应 |
20.烧杯中盛有含Mg2+、Al3+、Fe3+、Na+、Fe2+、Cl-六种离子的溶液,若向其中加入足量的Na2O2搅拌,充分反应后再向该烧杯中滴加足量的稀盐酸,此时上述离子物质的量保持不变的有( )
| A. | 1 种 | B. | 2 种 | C. | 3 种 | D. | 4种 |
7.现有25℃的下列四种溶液,其中碱性最强的是( )
| A. | pH=11的溶液 | B. | 4 g NaOH溶于水形成1L的水溶液 | ||
| C. | c(OH-)=0.12 mol•L-1 | D. | c(H+)=1×10-10 mol•L-1的溶液 |
4.除去下列物质中所含的杂质.选用的试剂正确的是( )
| 选项 | 物质(杂质) | 试剂 |
| A | Al2O3(SiO2) | 过量NaOH溶液 |
| B | CO2(HCl) | 饱和Na2CO3溶液 |
| C | Na2O2(Na2O) | O2/加热 |
| D | Al2O3(Fe2O3) | Al粉/加热 |
| A. | A | B. | B | C. | C | D. | D |
5.氮气是一种不活泼的气体,其根本原因是( )
| A. | 氮元素的非金属性较弱 | B. | 氮原子半径较小 | ||
| C. | 氮气是双原子分子 | D. | 使N≡N键断裂需要很高的能量 |