题目内容
10.已知Ag2SO4的Ksp=c2(Ag+)×c(SO42-)=1.4×10-5,将适量Ag2SO4固体溶于100mL水中至刚好饱和,[饱和Ag2SO4溶液中c(Ag+)=0.032mol•L-1].若t1时刻在上述体系中加入100mL相应溶液,下列示意图中,不能正确表示t1时刻后Ag+和SO42-浓度随时间变化关系的是( )| A. |  蒸馏水 | B. | 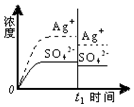 0.010mol•L-1 Ag2SO4溶液 | ||
| C. | 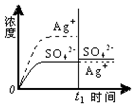 0.020mol•L-1 Na2SO4溶液 | D. | 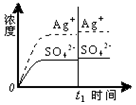 0.040mol•L-1 AgNO3溶液 |
分析 将适量Ag2SO4固体溶于100mL水中至刚好饱和,Ag2SO4刚好为100ml的饱和溶液,因为c(Ag+)=0.032mol•L-1,所以c(Ag2SO4)=0.0151mol•L-1;
A.加入100mL蒸馏水,溶液浓度减小;
B.已知c(Ag2SO4)=0.015mol•L-1;加入100mL 0.010mol•L-1 Ag2SO4,溶液浓度减小,银离子和硫酸根离子浓度都减小;
C.加入100mL 0.020mol•L-1 Na2SO4溶液,根据Qc与Ksp的相对大小分析溶液的变化;
D.加入100mL 0.040mol•L-1 AgNO3溶液,根据Qc与Ksp的相对大小分析溶液的变化.
解答 解:将适量Ag2SO4固体溶于100mL水中至刚好饱和,Ag2SO4刚好为100ml的饱和溶液,因为c(Ag+)=0.032mol•L-1,所以c(Ag2SO4)=0.0151mol•L-1;
A.加入100mL蒸馏水,溶液浓度减小,银离子浓度和硫酸根离子浓度都减小,大约为原来浓度的一半,故A正确;
B.已知c(Ag2SO4)=0.0151mol•L-1;加入100mL 0.010mol•L-1 Ag2SO4,溶液浓度减小,银离子浓度和硫酸根离子浓度都减小,故B正确;
C.加入100mL 0.020mol•L-1 Na2SO4溶液后,
c(Ag+)=$\frac{1}{2}$×0.032mol•L-1=0.0151mol•L-1,
c(SO42-)=(0.0151mol•L-1+0.02mol•L-1)×$\frac{1}{2}$=0.01755mol•L-1,
Qc=(0.0151mol•L-1)2×0.01755mol•L-1=4.0×10-6<Ksp=1.4×10-5,
所以没有沉淀析出,银离子浓度减小,硫酸根离子浓度增大,故C正确;
D.加入100mL 0.040mol•L-1 AgNO3溶液,c(Ag+)=$\frac{1}{2}$×(0.031mol•L-1+0.040mol•L-1)=0.0355mol•L-1,
c(SO42-)=$\frac{1}{2}$×0.0151mol•L-1=0.00755mol•L-1,
Qc=(0.0355mol•L-1)2×0.00755mol•L-1=9.5×10-6<Ksp=1.4×10-5,
所以没有沉淀析出,银离子浓度增大,硫酸根离子浓度减小,图中银离子浓度和硫酸根离子浓度都增大,故D错误;
故选:D.
点评 本题考查本题考查了溶度积常数的有关计算,题目难度中等,要求学生掌握溶度积常数的基本概念以及简单应用,通过比较溶度积与离子积的相对大小,可以判断难溶电解质在给定条件下沉淀能否生成或溶解,侧重于考查学生的分析能力和计算能力.

 有关苏糖的说法不正确的是( )
有关苏糖的说法不正确的是( )| A. | 苏糖能发生银镜反应 | |
| B. | 苏糖属于单糖 | |
| C. | 苏糖在一定条件下,能发生加成和取代反应 | |
| D. | 苏糖与葡萄糖互为同分异构体 |
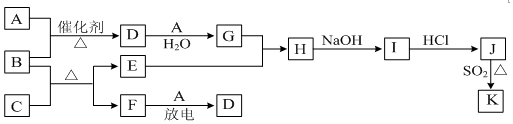
 碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.
碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.(1)真空碳热还原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
2Al2O3(s)+2AlCl3(g)+6C(s)=6AlCl(g)+6CO(g)△H=a kJ•mol-1
3AlCl(g)=2Al(l)+AlCl3(g)△H=b kJ•mol-1
反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H=0.5a+bkJ•mol-1(用含a、b的代数式表示);
(2)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)?N2(g)+CO2(g)△H=Q kJ•mol-1在T1℃时,反应进行到不同时间测得各物质的浓度如下:
| 时间(mol/L) 浓度(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是ad(填字母编号).
a.通入一定量的NO b.加入一定量的活性炭
c.加入合适的催化剂 d.适当缩小容器的体积
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3:1:1,则Q<0(填“>”或“<”).
④在恒容条件下,能判断该反应一定达到化学平衡状态的依据是bc(填选项编号).
a.单位时间内生成2n mol NO(g)的同时消耗n mol CO2(g)
b.反应体系的温度不再发生改变
c.混合气体的密度不再发生改变
d.反应体系的压强不再发生改变
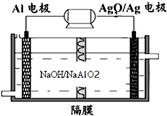
(3)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,其原理如图所示:
请写出该电池正极反应式Ag2O+2e-+H2O=2Ag+2OH-;常温下,用该化学电源和惰性电极电解300ml硫酸铜溶液(过量),消耗27mg Al,则电解后溶液的pH=2(不考虑溶液体积的变化).
| A. | 反应速率:前者快,后者慢 | |
| B. | 消耗硝酸的物质的量:前者多,后者少 | |
| C. | 反应生成相同条件下气体的体积:前者多,后者少 | |
| D. | 反应中转移的电子总数:前者多,后者少 |
| A. | 向Al2(SO4)3溶液中加入过量NH3•H2O:Al3++4NH3•H2O═-+4NH4+ | |
| B. | 铅酸蓄电池充电时的正极反应:PbO2+4H++SO42-+2e-═PbSO4+2H2O | |
| C. | Fe2(SO4)3溶液与Ba(OH)2溶液反应:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ | |
| D. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:2NH4++Fe2++4OH-═Fe(OH)2↓+2NH3•H2O |
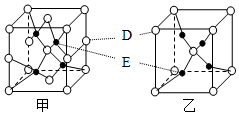 A、B、C、D、E五种元素的原子序数依次增大.A是原子半价最小的元素;B的最外层电子数是次外层电子数的2倍; D的L能层有两对成对电子;E+的核外有三个能层,且都外于全满状态.试回答下列问题:
A、B、C、D、E五种元素的原子序数依次增大.A是原子半价最小的元素;B的最外层电子数是次外层电子数的2倍; D的L能层有两对成对电子;E+的核外有三个能层,且都外于全满状态.试回答下列问题: