题目内容
20.氯碱工业是以电解饱和食盐水为基础的工业.饱和食盐水是以含Ca2+、Mg2+、SO42-、Fe3+等杂质离子的粗盐水精制,需要使用的药品包括:①稀盐酸 ②烧碱溶液 ③碳酸钠溶液 ④氯化钡溶液.下列有关说法不正确的是( )| A. | 加入烧碱溶液主要是除去Mg2+、Fe3+ | |
| B. | 药品加入的先后顺序可以是②③④① | |
| C. | 加入稀盐酸主要是除去所加过量物质中的OH-、CO32- | |
| D. | 加入碳酸钠溶液主要是除去Ca2+及所加过量物质中的Ba2+ |
分析 饱和食盐水含Ca2+、Mg2+、SO42-、Fe3+等杂质离子,应先加入过量BaCl2,除去SO42-,然后加过量Na2CO3,可除去Ca2+、Mg2+、Fe3+等,过滤后加入盐酸可除去Na2CO3,除钡离子要放在除碳酸根离子前,据此回答.
解答 解:饱和食盐水含Ca2+、Mg2+、SO42-、Fe3+等杂质离子,应先加入过量BaCl2,除去SO42-,然后加过量Na2CO3,可除去Ca2+、Mg2+、Fe3+等,过滤后加入盐酸可除去Na2CO3.
A、加入烧碱溶液主要是除去Mg2+、Fe3+,故A正确;
B、药品加入的先后顺序可以是②④③①,除钡离子要放在除碳酸根离子前,故B错误;
C、加入稀盐酸主要是除去所加过量物质中的OH-、CO32-,放在最后,故C正确;
D、加入碳酸钠溶液主要是除去Ca2+及所加过量物质中的Ba2+,故D正确.
故选B.
点评 本题考查了原电池和电解池原理的综合应用,涉及饱和食盐水的精制、电解方程式、电极方程式等知识,要求学生具有分析和解决问题的能力,题目难度中等.

练习册系列答案
相关题目
11.某温度下,液氨的离子积常数K=c(NH4+)•c(NH2-)=1.6×10-29,若用定义pH一样来规定pN=-lg c(NH4+),则在该温度下,下列叙述正确的是( )
| A. | 纯净的液氨中,pN=7 | |
| B. | 纯净的液氨中,c(NH4+)•c(NH2-)>1.0×10-14 | |
| C. | 1 L溶解有0.001 mol NH4C1的液氨溶液,其pN=3 | |
| D. | 1 L溶解有0.001 mol NaNH2的液氨溶液,其pN=11 |
8.某溶液中加入铝片有氢气产生,则该溶液中一定能大量共存的离子组是( )
| A. | Cl-、Fe3+ | B. | HCO3-、Al3+ | C. | Ba2+、SO42- | D. | Na+、SO42- |
15.在有机合成中,常会将官能团消除或增加,下列相关过程中反应类型及相关产物不合理的是( )
| A. | 乙烯 乙二醇: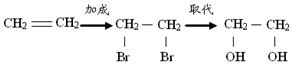 | |
| B. | 溴乙烷 乙醇:CH3CH2Br$\stackrel{水解}{→}$CH2═CH2$\stackrel{加成}{→}$CH3CH2OH | |
| C. | 1-溴丁烷 1,3-丁二烯: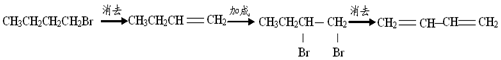 | |
| D. | 乙烯 乙炔: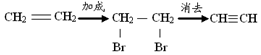 |
5.如图所示,下列实验操作与方法不正确的是( )
| A. | 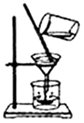 过滤 | B. | 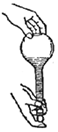 检查容量瓶是否漏水 | ||
| C. | 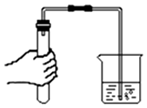 气密性检查 | D. | 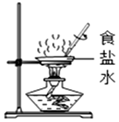 蒸发 |
12.己知下列几个反应的化学方程式:
①2FeCl2+Cl2═2FeCl3
②2FeCl3+2HI═2FeCl2+I2+2HCl
③I2+Na2S═2NaI+S
下列有关物质的氧化性的强弱排列顺序中正确的是( )
①2FeCl2+Cl2═2FeCl3
②2FeCl3+2HI═2FeCl2+I2+2HCl
③I2+Na2S═2NaI+S
下列有关物质的氧化性的强弱排列顺序中正确的是( )
| A. | Cl2>Fe3+>I2>S | B. | Cl2>I2>Fe3+>S | C. | Cl2>Fe3+>S>I2 | D. | Fe3+>I2>C12>S |
15.一定温度下,在Ba(OH)2的悬浊液中,存在Ba(OH)2固体与其电离的离子间的溶解平衡关系:Ba(OH)2(s)?Ba2+(aq)+2OH-(aq) 向此体系中再加入少量的BaO粉末,如果保持温度不变,则下列说法正确的是( )
| A. | c(Ba2+)浓度增大 | B. | 溶液中Ba2+数目减少 | ||
| C. | 溶液pH减小 | D. | 溶液pH增大 |