题目内容
下列化学用语表达正确的是( )
A、磷原子的原子结构示意: |
B、钠离子的电子式: |
C、甲烷的结构式: |
| D、质子数为8,中子数为10的核素:10O |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.P的质子数为15,带正电荷;
B.钠离子符合即为电子式;
C.甲烷中存在4个C-H键;
D.质子数为8,中子数为10的核素,质量数为8+10=18.
B.钠离子符合即为电子式;
C.甲烷中存在4个C-H键;
D.质子数为8,中子数为10的核素,质量数为8+10=18.
解答:
解:A.P的质子数为15,带正电荷,则磷原子的原子结构示意为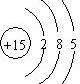 ,故A错误;
,故A错误;
B.钠离子符合即为电子式,则钠离子的电子式为Na+,故B错误;
C.甲烷中存在4个C-H键,则甲烷的结构式为 ,故C正确;
,故C正确;
D.质子数为8,中子数为10的核素,质量数为8+10=18,则核素为
O,故D错误;
故选C.
 ,故A错误;
,故A错误;B.钠离子符合即为电子式,则钠离子的电子式为Na+,故B错误;
C.甲烷中存在4个C-H键,则甲烷的结构式为
 ,故C正确;
,故C正确;D.质子数为8,中子数为10的核素,质量数为8+10=18,则核素为
18 8 |
故选C.
点评:本题考查化学用语的综合应用,涉及电子式、结构式、结构示意图及原子的表示方法等,为基础性习题,把握化学用语的区别及规范应用为解答的关键,题目难度不大.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
下列叙述正确( )
| A、标准状况下,1mol任何物质的体积约为22.4L |
| B、1mol气体的体积约为22.4L |
| C、1mol氖气和1mol氧气体积相同 |
| D、标准状况下,1mol 空气的体积约为22.4L |
下列用量不正确的是( )
| A、没有说明用量,液体取2mL-4mL | ||
B、酒精灯的酒精不超过容积的
| ||
C、加热时,液体不超过试管的
| ||
| D、洗涤试管时,注入半试管水 |
下列物质中属于纯净物的是( )
| A、洁净的食盐水 |
| B、冰水混合物 |
| C、净化后的空气 |
| D、高锰酸钾完全分解后的剩余物 |
下列离子方程式中正确的是( )
| A、H2SO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
| B、Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
| C、NaOH溶液中通入少量CO2:CO32-+CO2+H2O═2HCO3- |
| D、CH3COOH溶液与NaOH溶液反应:H++OH-═H2O |
短周期元素的离子aW2+、bX+、cY2-、dZ-都具有相同的电子层结构,则下列推断正确的是( )
| A、碱性:XOH>W(OH)2 |
| B、热稳定性:H2Y>HZ |
| C、离子半径:W2+>Y2- |
| D、原子半径:W>X>Y>Z |
下列关于铁的叙述错误的是( )
| A、可以用KSCN溶液检验Fe3+的存在 |
| B、铁位于元素周期表中的第四周期第ⅧB族 |
| C、在人体的血红蛋白中含有铁元素 |
| D、能通过化合反应制得FeCl2和Fe(OH)3 |
硼烷是一种潜在的高能燃料,工业制取可用反应:B2O3+2Al+3H2
Al2O3+B2H6,下列有关说法正确的是( )
| ||
| 高压 |
| A、该反应中氢气做还原剂,铝做氧化剂 |
| B、在空气中Al2O3比B2H6更稳定 |
| C、B2H6中存在极性键、非极性键、离子键 |
| D、每生成1mol B2H6要消耗2mol B2O3 |
下列依据热化学方程式得出的结论正确的是( )
| A、已知2H2(g)+O2(g)=2H2O(l)△H=-483.6 kJ?mol-1,则氢气的燃烧热为483.6 kJ?mol-1 |
| B、已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 |
| C、已知2C(s)+2O2(g)=2CO2(g)△H1 2C(s)+O2(g)=2CO(g)△H2 则△H1>△H2 |
| D、已知Ni(CO)4(s)=Ni(s)+4CO(g)△H=Q kJ?mol-1,则Ni(s)+4CO(g)=Ni(CO)4(s)△H=-Q kJ?mol-1 |