题目内容
17.检验某无SO42-的溶液中是否含有Cl-,正确的操作是( )| A. | 取样,滴加AgNO3溶液,看是否有白色沉淀 | |
| B. | 取样,先加盐酸酸化,再加入AgNO3溶液,看是否有白色沉淀生成 | |
| C. | 取样,加少量AgNO3溶液,有白色沉淀,再加稀HCl,看白色沉淀是否消失 | |
| D. | 取样,加少量AgNO3溶液,有白色沉淀,再加稀HNO3,看白色沉淀是否消失 |
分析 因为AgCl不溶于水,不溶于稀硝酸,因此,在检验Cl-时,要加入硝酸银溶液,但是CO32- 等离子也能与硝酸银生成沉淀,但能溶于稀硝酸,因此,在加入硝酸银之前,一定要加入稀硝酸来除去CO32-等离子,以此来解答.
解答 解:不能加盐酸酸化或观察沉淀的溶解,将引入氯离子,干扰检验;
则检验某无SO42-的溶液中是否含有Cl-,取样,加少量AgNO3溶液,有白色沉淀,再加稀HNO3,看白色沉淀是否消失,白色沉淀不消失可说明含Cl-,
故选D.
点评 本题考查离子的检验,为高频考点,把握离子检验的试剂、现象与结论为解答的关键,侧重分析与应用能力的考查,注意离子检验时排除干扰离子,题目难度不大.

练习册系列答案
相关题目
7.Ge 和Sn 的熔点( )
| A. | 大于 | B. | 小于 | C. | 等于 | D. | 不能肯定 |
5.关于氧化还原反应和离子反应,下列说法正确的是( )
①金属在反应中只能作还原剂,非金属在反应中只能作氧化剂;
②氧化剂发生氧化反应;
③还原剂失去电子,化合价升高;
④溶液中的离子反应不可能是氧化还原反应;
⑤发生离子反应后,溶液的导电性减弱.
①金属在反应中只能作还原剂,非金属在反应中只能作氧化剂;
②氧化剂发生氧化反应;
③还原剂失去电子,化合价升高;
④溶液中的离子反应不可能是氧化还原反应;
⑤发生离子反应后,溶液的导电性减弱.
| A. | ①②④ | B. | ①③⑤ | C. | ②③⑤ | D. | 只有③ |
2. 某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题:
某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题:
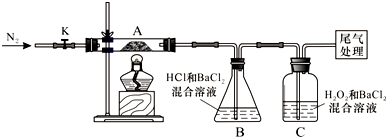
(1)铝热反应实验:取磁性氧化铁粉按课本中的实验装置(如图)进行铝热反应,将反应
后所得“铁块”溶于盐酸,向反应后的溶液中滴加KSCN溶液,发现溶液变血红色.
①出现这种现象的原因,除了因“铁块”中可能混有没反应完的磁性氧化铁外,还有一种可能原因是熔融的铁被空气中氧气氧化.
②若要证明反应所得“铁块”中含有金属铝,可用(填化学式)溶液,所发生反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(2)化学反应速率影响因素的探究实验:
KI在经酸化的溶液中被空气氧化的反应式为:4H++4I-+O2=2I2+2H2O.该反应的速率受温度、酸度、溶剂、试剂浓度等影响,可用淀粉与碘的显色反应来观测该反应的速率.已知,淀粉与碘的显色反应在温度升高时灵敏度会降低,高于75℃则不能显色;淀粉浓度越高显色越灵敏、颜色也越深.
实验小组拟用0.8mol•L-1 KI溶液、0.1mol•L-1H2SO4溶液、淀粉溶液等来探究温度、酸度对上述反应速率的影响,他们做了A-C三组实验,部分实验数据如下表:
①为确保A组实验在39℃下进行,应采用的控温操作方法是量出的各种溶液分别装在试管中,再将试管全部放在同一水浴中加热,用温度计测量试管中溶液的温度.
②A-C三组实验时,都加入了5mL水,其目的是为了在后续研究酸度因素对反应速率影响时保持KI和淀粉浓度不变.
③B组实验中“没出现蓝色”,原因是温度(TB)高于75℃,淀粉与碘不显色.
④请你为小组设计D组实验方案(在表格空白处填入你设计的5个数据),以帮助小组完成探究目标.
⑤按你设计的实验数据,请你预测一个t值,并写出与你预测相对应的探究实验结论.
 某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题:
某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题:(1)铝热反应实验:取磁性氧化铁粉按课本中的实验装置(如图)进行铝热反应,将反应
后所得“铁块”溶于盐酸,向反应后的溶液中滴加KSCN溶液,发现溶液变血红色.
①出现这种现象的原因,除了因“铁块”中可能混有没反应完的磁性氧化铁外,还有一种可能原因是熔融的铁被空气中氧气氧化.
②若要证明反应所得“铁块”中含有金属铝,可用(填化学式)溶液,所发生反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(2)化学反应速率影响因素的探究实验:
KI在经酸化的溶液中被空气氧化的反应式为:4H++4I-+O2=2I2+2H2O.该反应的速率受温度、酸度、溶剂、试剂浓度等影响,可用淀粉与碘的显色反应来观测该反应的速率.已知,淀粉与碘的显色反应在温度升高时灵敏度会降低,高于75℃则不能显色;淀粉浓度越高显色越灵敏、颜色也越深.
实验小组拟用0.8mol•L-1 KI溶液、0.1mol•L-1H2SO4溶液、淀粉溶液等来探究温度、酸度对上述反应速率的影响,他们做了A-C三组实验,部分实验数据如下表:
| 编号 | 温度/℃ | H2SO4体积/mL | KI溶液体积/mL | H2O体积/mL | 淀粉溶液 /mL | 出现蓝色时间/s |
| A | 39 | 10 | 5 | 5 | 1 | 5 |
| B | TB | 10 | 5 | 5 | 1 | 没出现蓝色 |
| C | 5 | 10 | 5 | 5 | 1 | 39 |
| D | t |
②A-C三组实验时,都加入了5mL水,其目的是为了在后续研究酸度因素对反应速率影响时保持KI和淀粉浓度不变.
③B组实验中“没出现蓝色”,原因是温度(TB)高于75℃,淀粉与碘不显色.
④请你为小组设计D组实验方案(在表格空白处填入你设计的5个数据),以帮助小组完成探究目标.
⑤按你设计的实验数据,请你预测一个t值,并写出与你预测相对应的探究实验结论.
9.浓硫酸与下列物质作用时,既表现氧化性,又表现酸性的是( )
①炽热的木炭 ②H2S气体 ③Cu ④FeO ⑤NH3 ⑥蔗糖 ⑦CuSO4•5H2O ⑧铁、铝.
①炽热的木炭 ②H2S气体 ③Cu ④FeO ⑤NH3 ⑥蔗糖 ⑦CuSO4•5H2O ⑧铁、铝.
| A. | ③④ | B. | ①②⑤⑧ | C. | ①②③④⑦ | D. | ⑥⑦ |
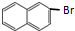 .
.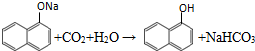 ;
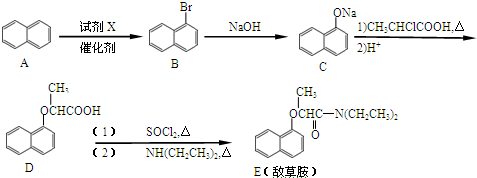
;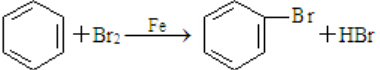 、C6H5Br+NaOH$→_{△}^{水}$C6H5OH+NaBr、C6H5ONa+CO2+H2O→C6H5OH+NaHCO3.
、C6H5Br+NaOH$→_{△}^{水}$C6H5OH+NaBr、C6H5ONa+CO2+H2O→C6H5OH+NaHCO3.