题目内容
9.在同温同压下,密度相同的气体组是( )| A. | CO NO | B. | NO C2H6 | C. | C2H4 N2 | D. | SO2 Cl2 |
分析 同温同压下,气体的密度之比等于其相对分子质量之比.
解答 解:同温同压下,气体的密度之比等于其相对分子质量之比.
A.CO、NO的相对分子质量不相等,同温同压下二者密度不相等,故A不符合;
B.NO、C2H6的相对分子质量均为30,同温同压下二者密度相等,故B符合;
C.C2H4、N2的相对分子质量均为28,同温同压下二者密度相等,故C符合;
D.SO2、Cl2的相对分子质量不相等,同温同压下二者密度不相等,故D不符合.
故选:BC.
点评 本题考查阿伏伽德罗定律及其推论的应用,注意根据PV=nRT理解阿伏伽德罗定律及其推论.

练习册系列答案
相关题目
19.下表列出了A~R九种元素在周期表的位置:
(1)写出EF2分子的电子式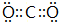 .
.
(2)A、C、D三种元素的最高价氧化物对应的水化物中碱性最强的是NaOH (填化学式).
(3)H、I、G三种元素的最高价氧化物对应的水化物中酸性由大到小的顺序排列为Cl>S>Si.(只填写元素符号)
(4)写出A的单质与水反应的化学方程式2Na+2H2O=2NaOH+H2↑.
(5)H在元素周期表中位置第3周期第IVA族:
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | E | R | F | |||||
| 3 | A | C | D | H | I | G | ||
| 4 | B |
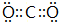 .
.(2)A、C、D三种元素的最高价氧化物对应的水化物中碱性最强的是NaOH (填化学式).
(3)H、I、G三种元素的最高价氧化物对应的水化物中酸性由大到小的顺序排列为Cl>S>Si.(只填写元素符号)
(4)写出A的单质与水反应的化学方程式2Na+2H2O=2NaOH+H2↑.
(5)H在元素周期表中位置第3周期第IVA族:
20.下列对离子方程式的评价不正确的是( )
| 离子方程式 | 评价 |
| A.亚磷酸是一种二元酸,在其中加入过量的烧碱溶液: H3PO3+3OH-=PO33-+3H2O | 正确 |
| B.在亚硫酸中加入少量的次氯酸钠溶液 H2SO3+ClO-=Cl-+2H++SO42- | 正确 |
| C.在碳酸氢镁溶液中加入过量氢氧化钠溶液: Mg2++2HCO3-+2OH-=Mg CO3↓+CO32-+2H2O | 错误:生成物应是 Mg(OH)2和Na2CO3 |
| D.在过氧化钠中加入稀硫酸: 2Na2O2+4H+=4Na++2H2O+O2↑ | 正确 |
| A. | A | B. | B | C. | C | D. | D |
4.X盐和Y酸反应可生成Z,Z跟NaOH反应又可得盐X,Z氧化的最终产物为W,W溶于水后又得酸Y,则X盐和Y酸为( )
| A. | Na2CO3和H2SO4 | B. | Na2SO3和盐酸 | C. | Na2S和HCl | D. | Na2SO3和H2SO4 |
14.用NA代表阿伏加德罗常数的值,下列有关说法正确的是( )
| A. | 78g过氧化钠晶体中,含2NA个阴离子 | |
| B. | 常温常压下,22.4L氦气含有NA个氦原子 | |
| C. | 在H2O2参与的反应中,1 mol H2O2得到或失去的电子数一定是2NA | |
| D. | 常温下16g O2与O3的混合气体中含氧原子数为NA |
1.可用来鉴别乙烯、四氯化碳、苯的试剂是( )
| A. | 酸性高锰酸钾 | B. | 溴水 | ||
| C. | 液溴 | D. | 浓硝酸和浓硫酸混合液 |
18.用NA表示阿伏德罗常数的值,下列叙述正确的是( )
| A. | 18gD2O中含有的质子数目为10NA | |
| B. | 12.0 g熔融的NaHSO4中含有0.1NA个Na+、0.1NA个H+和0.1NA个SO42- | |
| C. | 氢氧燃料电池工作时,若负极反应0.5g H2时,则正极反应的O2的体积(折算为标况)是2.8L | |
| D. | 22.4LNH3分子中含有的共价键数目为3NA |