题目内容
5.某化学兴趣小组拟用粗氧化铜(含少量铜粉、氧化铁及不溶于酸的杂质)制取无水氯化铜,其制备步骤如下
实验过程中所用的物质x,y及pH控制参照下表确定:表I
| 物质 | 开始沉淀时pH | 完全沉淀时pH |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 5.2 | 6.4 |
| 氧化剂 | 调节pH的物质 | ||
| A | 双氧水 | E | 氨水 |
| B | 高锰酸钾 | F | 碱式碳酸铜 |
| C | 氯水 | G | 氧化铜 |
(1)沉淀Ⅱ的成分(化学式)是Fe(OH)3.
(2)步骤②加入的试剂x可选用表Ⅱ中的AC (填序号,且选出全部合理的),其作用是将亚铁离子转化为铁离子
(3)步骤③加入的试剂y可选用表Ⅱ中的FG(填序号,且选出全部合理的),控制pH=5的目的是将铁离子转化为沉淀而铜离子不产生沉淀
(4)步骤⑤要得到无水CuCl2,应控制的一定条件是在干燥的HCl气流中加热CuCl2•2H2O.
(5)步骤①中所发生的全部反应的离子方程式:CuO+2H+=Cu2++H2O、Fe2O3+6H+=2Fe3++3H2O、Cu+2Fe3+=Cu2++2Fe2+.
分析 粗氧化铜中含CuO(含少量Cu、Fe2O3及不溶于酸的杂质),加入过量盐酸,CuO和盐酸反应方程式为CuO+2HCl=CuCl2+H2O,氧化铁和稀盐酸反应方程式为Fe2O3+6HCl=2FeCl3+3H2O,Cu和铁离子反应Cu+2Fe3+=Cu2++2Fe2+,过滤,溶液Ⅰ中含Fe3+、Fe+、Cu2+、H+、Cl-;
从实验目的来看,应把铁元素除去,调节pH=5,只有Fe3+沉淀,Fe2+不沉淀,故应先把Fe2+氧化成Fe3+,故加入的X为氧化剂,为了不引入新的杂质,可选用H2O2或氯水,溶液Ⅱ含Fe3+、Cu2+、H+等阳离子;加入Y是调节pH,从不引入杂质考虑,应选用含Cu的化合物,沉淀Ⅱ为Fe(OH)3,溶液Ⅲ中含Cu2+和Cl-,蒸发浓缩、冷却结晶、过滤、洗涤得到CuCl2晶体;在氯化氢氛围中加热CuCl2晶体得到无水CuCl2;
(1)沉淀II是氢氧化铁;
(2)操作②是加入氧化剂把亚铁离子氧化为铁离子;
(3)调节溶液的pH目的是使铁离子全部沉淀,铜离子不沉淀,但不能引入新的杂质;
(4)控制条件抑制氯化铜的水解,以便得到氯化铜晶体;
(5)该操作中CuO、氧化铁都溶于稀盐酸,且Cu还和铁离子反应.
解答 解:粗氧化铜中含CuO(含少量Cu、Fe2O3及不溶于酸的杂质),加入过量盐酸,CuO和盐酸反应方程式为CuO+2HCl=CuCl2+H2O,氧化铁和稀盐酸反应方程式为Fe2O3+6HCl=2FeCl3+3H2O,Cu和铁离子反应Cu+2Fe3+=Cu2++2Fe2+,过滤,溶液Ⅰ中含Fe3+、Fe+、Cu2+、H+、Cl-;
从实验目的来看,应把铁元素除去,调节pH=5,只有Fe3+沉淀,Fe2+不沉淀,故应先把Fe2+氧化成Fe3+,故加入的X为氧化剂,为了不引入新的杂质,可选用H2O2或氯水,溶液Ⅱ含Fe3+、Cu2+、H+等阳离子;加入Y是调节pH,从不引入杂质考虑,应选用含Cu的化合物,沉淀Ⅱ为Fe(OH)3,溶液Ⅲ中含Cu2+和Cl-,蒸发浓缩、冷却结晶、过滤、洗涤得到CuCl2晶体;在氯化氢氛围中加热CuCl2晶体得到无水CuCl2;
(1)沉淀Ⅱ的成分(化学式)是Fe(OH)3,故答案为:Fe(OH)3;
(2)步骤②加入的试剂x可选用表Ⅱ中的 操作②是加入氧化剂把亚铁离子氧化为铁离子但不能引入新的杂质,
A.双氧水还原产物为水,不会引入新的杂质,可选;
B.高锰酸钾还原产物为锰离子,还有钾离子,引入了新的杂质,不选;
C.氯气的还原产物为氯离子,不会引入新的杂质,可选;
D.硝酸还原产物为氮的氧化物,会造成污染,且过量硝酸会引入硝酸根离子,不选;
故答案为:AC;将亚铁离子转化为铁离子;
(3)加入氨水可调节pH,但引入了新的杂质铵根离子,铜的化合物氧化铜、碱式碳酸铜、氢氧化铜都可和氢离子反应,能调节pH,且不会引入新的杂质;调节溶液的pH=5能将铁离子转化为沉淀而铜离子不产生沉淀,故答案为:FG;将铁离子转化为沉淀而铜离子不产生沉淀;
(4 ) 步骤⑤要得到无水氯化铜,需要在干燥的HCl气流中加热CuCl2•2H2O,是为了抑制铜离子的水解得到氯化铜晶体同时带走产生的水蒸气,
故答案为:在干燥的HCl气流中加热CuCl2•2H2O;
(5)该操作中CuO、氧化铁都溶于稀盐酸,且Cu还和铁离子反应,离子方程式有CuO+2H+=Cu2++H2O、Fe2O3+6H+=2Fe3++3H2O、Cu+2Fe3+=Cu2++2Fe2+,
故答案为:CuO+2H+=Cu2++H2O、Fe2O3+6H+=2Fe3++3H2O、Cu+2Fe3+=Cu2++2Fe2+.
点评 本题考查物质制备,为高频考点,涉及物质分离和提纯、氧化还原反应、基本操作等知识点,综合性较强,明确流程图中发生的反应及基本操作方法是解本题关键,注意题给信息的选取和运用,题目难度不大.

 每课必练系列答案
每课必练系列答案①I-、Cl-、Ba2+、NO3-
②Na+、NO3-、K+、CO32-
③K+、SO42-、Na+、AlO2-
④HCO3-、NO3-、Al3+、SO42-.
| A. | 只有①④ | B. | 只有②③ | C. | ①②③ | D. | ①②③④都不能 |
| A. | H2O2的电子式 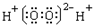 | |
| B. | 氨分子的结构式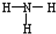 | |
| C. | S2-的结构示意图 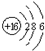 | |
| D. | 原子核内有20个中子的氯原子${\;}_{37}^{17}Cl$ |
| A. | 物质的量就是物质的质量 | |
| B. | 2mol H2O 可以说为水分子的摩尔数为2mol | |
| C. | 物质的量是以摩尔为单位计量粒子数目的物理量 | |
| D. | 物质的量和摩尔都是含有一定数目粒子的集体 |
| A. | NH4+、NO3-、Al3+、Cl- | B. | Na+、OH-、K+、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | K+、SO42-、HCO3-、Na+ |
| A. | CH3CH=CH2+Br2$\stackrel{CCl_{4}}{→}$CH3CHBrCH2Br | |
| B. | CH3CH2OH $→_{170℃}^{浓H_{2}SO_{4}}$ CH2=CH2↑+H2O | |
| C. | CH3COOH+CH3CH2OH $→_{△}^{浓H_{2}SO_{4}}$ CH3COOCH2CH3+H2O | |
| D. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O |
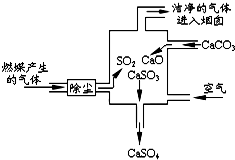
| A. | 此过程中没有分解反应 | |
| B. | 整个过程的反应可表示为:2SO2+2CaCO3+O2═2CaSO4+2CO2 | |
| C. | 使用此废气处理装置可减少CO2的排放 | |
| D. | 此过程中S元素的化合价未发生改变 |
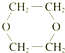 的方案.依次写出合成方案中所涉及反应的化学方程式.
的方案.依次写出合成方案中所涉及反应的化学方程式.