题目内容
8.下列说法正确的是( )| A. | 在100℃、101 kPa条件下,液态水的气化热为40.69 kJ•mol-1,则H2O(g)?H2O(l) 的△H=40.69 kJ•mol-1 | |||||||||||
| B. | 已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)•c(CO32-)=6.82×10-6 | |||||||||||
| C. | 已知:
| |||||||||||
| D. | 已知CaCO3 (s)?CaO(s)+CO2(g)△H>0,则低温有利于该反应的自发进行 |
分析 A、液态水的气化热为40.69kJ•mol-1,是液体水变化为气体需要吸收热量,焓变为负值;
B、c(Mg2+)•c(CO32-)=“6.82“×10-6,但不一定都有c(Mg2+)=c(CO32-);
C、反应焓变=反应物键能总和-生成物键能总和,结合热化学方程式书写方法写出;
D、反应自发进行的判断依据是△H-T△S<0.
解答 解:A、液态水的气化热为40.69kJ•mol-1,是液体水变化为气体需要吸收热量,焓变为负值,故A错误;
B、c(Mg2+)•c(CO32-)=“6.82“×10-6,但不一定都有c(Mg2+)=c(CO32-),温度不变存在c(Mg2+)•c(CO32-)=6.82×10-6,故B错误;
C、反应焓变=反应物键能总和-生成物键能总和=4×360+2×436-2×176-4×431=-236KJ/mol,反应热化学方程式为:SiCl4(g)+2H2(g) 高温 Si(s)+4 HCl(g),则该反应的△H=+236 kJ•mol-1,故C正确;
D、已知CaCO3 (s)?CaO(s)+CO2(g)△H>0,△S>0,△H-T△S<0;则高温△H-T△S<0,有利于该反应的自发进行,故D错误;
故选C.
点评 本题考查了反应热化学方程式的书写、计算,溶度积常数分析,注意焓变利用键能的计算应用,掌握基础是关键,题目难度中等.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
3.下列五组物质互为同素异形体的是( )
①16O2和18O2 ②H2SiO3和H4SiO4 ③O2和O3 ④H2O和H2O2 ⑤金刚石、石墨和C60 ⑥红磷和白磷.
①16O2和18O2 ②H2SiO3和H4SiO4 ③O2和O3 ④H2O和H2O2 ⑤金刚石、石墨和C60 ⑥红磷和白磷.
| A. | 只有②③⑤ | B. | 只有③⑤⑥ | C. | 只有①③⑤ | D. | 只有①②④⑥ |
4.下列实验操作正确的是( )
| 选项 | 实验 | 操作 |
| A | 验证Cl2和Br2的非金属性强弱 | 将少量氯水加入盛有FeBr2溶液的试管中,用力振荡后加入少量乙醇,振荡,静置 |
| B | 检验溶液中是否含有SO42- | 用HNO3溶液酸化后再加BaCl2溶液 |
| C | 证明浓硫酸有脱水性和强氧化性 | 将浓硫酸滴到蔗糖表面 |
| D | 制取Fe(OH)3胶体 | 将烧碱溶液滴加到FeCl2溶液中 |
| A. | A | B. | B | C. | C | D. | D |
16.下列除去括号内杂质的有关操作方法不正确的是( )
| A. | 淀粉溶液(NaCl):渗析 | |
| B. | 乙醇(乙酸):加NaOH溶液,分液 | |
| C. | 乙醛溶液(乙酸):加NaOH溶液,蒸馏 | |
| D. | 肥皂液(甘油):加食盐搅拌、盐析、过滤 |
3.某氮的氧化物是大气污染物之一,在一定温度和有催化剂的条件下,该氧化物与氨气反应只生成氮气和水,若生成的氮气和水的物质的量之比为5:6,该氧化物的化学式为( )
| A. | N2O5 | B. | NO | C. | NO2 | D. | N2O3 |
17.下列实验中,仪器的下端必须插入液面以下的是( )
①制备氢气的简易装置中加入稀硫酸的长颈漏斗
②制备氯气装置中的分液漏斗
③用新制的FeSO4溶液和NaOH溶液制备Fe(OH)2操作中的胶头滴管
④将氯气溶于水时制取氯水的导气管
⑤蒸馏石油时的温度计.
①制备氢气的简易装置中加入稀硫酸的长颈漏斗
②制备氯气装置中的分液漏斗
③用新制的FeSO4溶液和NaOH溶液制备Fe(OH)2操作中的胶头滴管
④将氯气溶于水时制取氯水的导气管
⑤蒸馏石油时的温度计.
| A. | ①③ | B. | ②④⑤ | C. | ①③④ | D. | 全部 |
18.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2 L三氧化硫所含有的原子数目为2NA | |
| B. | 分解H2O2制O2,每生成1mol O2转移2NA个电子 | |
| C. | 62 g Na2O溶于水后所得溶液中含有O2-数为NA | |
| D. | 36.5 g HCl中含有Cl-数为NA |
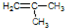 ,其系统命名为2-甲基-1-丙烯.
,其系统命名为2-甲基-1-丙烯.