题目内容
A、B、C、D、E是短周期元素,周期表中A与B、C与E相邻;A与E的最外层电子数之比2:3,B的最外层电子数比C的最外层电子数少1个;常见化合物D2C2与水反应生成C的单质,且溶液使酚酞试液变红.
(1)E的元素名称是 .该元素在周期表中的位置为
(2)A、B、C的氢化物稳定性由弱到强的顺序为(用分子式表示) ;B的氢化物和B的最高价氧化物的水化物反应生成Z,则Z中所含化学键的类型为
(3)写出D2C2的电子式 .
(1)E的元素名称是
(2)A、B、C的氢化物稳定性由弱到强的顺序为(用分子式表示)
(3)写出D2C2的电子式
考点:位置结构性质的相互关系应用
专题:
分析:根据常见化合物D2C2与水反应生成C的单质,且溶液使酚酞试液变红,可知C为O元素,D为Na元素,B的最外层电子数比C的最外层电子数少1个,则B的最外层电子数为5,A与B相邻,C与E相邻,A与E的最外层电子数之比2:3,则A的最外层电子数为4,应为C元素,B应为N元素,E应为S元素,根据元素所在周期表中的位置结合元素周期律的递变规律以及对应化合物的结构和性质解答该题.
解答:
解:根据常见化合物D2C2与水反应生成C的单质,且溶液使酚酞试液变红,可知C为O元素,D为Na元素,B的最外层电子数比C的最外层电子数少1个,则B的最外层电子数为5,A与B相邻,C与E相邻,A与E的最外层电子数之比2:3,则A的最外层电子数为4,应为C元素,B应为N元素,E应为S元素,
(1)E为S元素,原子序数为16,核外有3个电子层,最外层电子数为6,位于周期表第三周期VIA族,
故答案为:硫;第三周期VIA族;
(2)A、B、C分别为C、N、O元素,同一周期元素从左到右元素的非金属性逐渐增强,对应的氢化物的稳定性逐渐增大,A、B、C的氢化物稳定性由弱到强的顺序为CH4<NH3<H2O,B的氢化物和B的最高价氧化物的水化物反应生成Z,则Z为NH4NO3,为离子化合物,含有离子键、极性键,
故答案为:CH4<NH3<H2O;离子键、极性键;
(3)Na2O2为离子化合物,电子式为 ,
,
故答案为: ;
;
(1)E为S元素,原子序数为16,核外有3个电子层,最外层电子数为6,位于周期表第三周期VIA族,
故答案为:硫;第三周期VIA族;
(2)A、B、C分别为C、N、O元素,同一周期元素从左到右元素的非金属性逐渐增强,对应的氢化物的稳定性逐渐增大,A、B、C的氢化物稳定性由弱到强的顺序为CH4<NH3<H2O,B的氢化物和B的最高价氧化物的水化物反应生成Z,则Z为NH4NO3,为离子化合物,含有离子键、极性键,
故答案为:CH4<NH3<H2O;离子键、极性键;
(3)Na2O2为离子化合物,电子式为
 ,
,故答案为:
 ;
;
点评:本题考查原子结构与元素周期律的关系,题目难度中等,正确推断元素的种类为解答该题的关键,注意电子式的书写.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
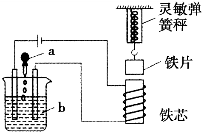 如图所示,向烧杯内的溶液b中逐渐加入溶液a时,灵敏弹簧秤的读数先逐渐变小然,然后又逐渐变大,则溶液a、b分别是( )
如图所示,向烧杯内的溶液b中逐渐加入溶液a时,灵敏弹簧秤的读数先逐渐变小然,然后又逐渐变大,则溶液a、b分别是( )| A、NaOH、H2SO4 |
| B、BaCl2、NaOH |
| C、Ba(OH)2、Na2SO4 |
| D、NH3?H2O、CH3COOH |
 室温下,用0.1mol/LHCl滴定10mL0.1mol/LNa2CO3,滴定曲线如图所示.下列说法正确的是( )
室温下,用0.1mol/LHCl滴定10mL0.1mol/LNa2CO3,滴定曲线如图所示.下列说法正确的是( )| A、水电离程度由大到小的顺序为:a>b>c>d |
| B、a点时:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) |
| C、b点时:3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) |
| D、d点时:c(H+)>c(HCO3-)=c(CO32-) |
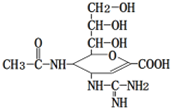 “甲型H7N9”流感疫情已构成“具有国际影响的公共卫生紧急事态”.已知扎那米韦是流感病毒神经氨酸酶抑制剂,其对流感病毒的抑制是以慢结合的方式进行的,具有高度特异性,其分子结构如图所示.下列说法正确的是( )
“甲型H7N9”流感疫情已构成“具有国际影响的公共卫生紧急事态”.已知扎那米韦是流感病毒神经氨酸酶抑制剂,其对流感病毒的抑制是以慢结合的方式进行的,具有高度特异性,其分子结构如图所示.下列说法正确的是( )| A、该物质的分子式为C12H19N4O7 |
| B、1mol该物质与NaOH溶液反应,可以消耗4molNaOH |
| C、在一定条件下,该物质可以发生消去、加成、取代等反应 |
| D、该物质能使溴水或高锰酸钾溶液褪色,能与FeCl3溶液发生显色反应 |
 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E元素+3价离子外围电子排布式为3d5.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E元素+3价离子外围电子排布式为3d5.回答下列问题: