题目内容
8.将8.8g FeS固体置于200mL 过量的盐酸中,以制备H2S气体.反应完全后,若溶液中H2S的浓度为0.10mol•L-1,假定溶液体积不变,试计算(计算结果均保留2位有效数字):(1)收集到的H2S气体的体积(标准状况).
(2)溶液中Fe2+的物质的量浓度.
分析 (1)先进行过量判断,然后根据方程式进行计算;
(2)先求出各自的物质的量然后代入公式C=$\frac{n}{v}$来解.
解答 解:(1)FeS的物质的量为$\frac{8.8g}{88g/mol}$=0.1mol,盐酸的物质的量为0.2L×2.0mol•L-1=0.4mol,根据方程式FeS+2H+═Fe2++H2S↑可判断盐酸过量,计算应以FeS的物质的量为基准,则共生成H2S 0.1mol.在溶液中溶解的物质的量为:0.10mol•L-1×0.2L=0.02mol,所以收集到的H2S气体的物质的量为0.08mol,其体积为:0.08mol×22.4L/mol=1.8L,
故答案为:收集到的H2S气体的体积(标准状况)为1.8L.
(2)参加反应的FeS的物质的量0.1mol,根据方程式FeS+2H+═Fe2++H2S↑得Fe2+的物质的量为0.1mol,所以Fe2+的物质的量浓度为$\frac{0.1mol}{0.2L}$=0.5mol•L-1故答案为:溶液中Fe2+的物质的量浓度为0.5mol•L-1.
点评 本题考查物质的量浓度的计算题目,难度不大,注意有关计算公式的运用.

练习册系列答案
相关题目
19.已知下述三个实验均能发生化学反应.
下列判断正确的是( )
| ① | ② | ③ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴浓硝酸 | 将铁钉放入氯化铁溶液中 |
| A. | 实验①和③中的铁钉只作还原剂 | |
| B. | 上述实验证明氧化性:Fe3+>Fe2+>Cu2+ | |
| C. | 实验②中,当转移0.2mol电子时,有0.1mol的Fe2+被氧化 | |
| D. | 实验③中反应的离子方程式为:Fe+Fe3+═2Fe2+ |
16.有机物甲的分子式为C7H14O2,在酸性条件下甲水解为乙和丙两种有机物,在相同的温度和压强下,同质量的乙和丙两种有机物的蒸气所占体积相同,则甲的可能结构为( )
| A. | 2 种 | B. | 4 种 | C. | 8 种 | D. | 16 种 |
13.X、Y、Z、W四种元素在周期表中相对位置如图,Y、Z质子数之和为21,下列说法正确的是( )
| X | Y | ||
| Z | W |
| A. | 常温下,四种元素单质中,全部是固体 | |
| B. | Z的阳离子与Y的阴离子电子层结构相同 | |
| C. | X的气态氢化物比Y的气态氢化物稳定 | |
| D. | W元素原子半径比Z元素原子半径大 |
20.下列物质与苯酚互为同系物的是( )
| A. | 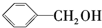 | B. | 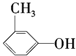 | C. | 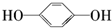 | D. | 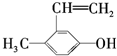 |
17.某有机物M的蒸气与相同状况下同体积氧气的质量比是30,其分子中碳、氢的质量分数分别是40%、6.6%,其余为氧.有机物M的分子式为( )
| A. | CH2O | B. | C2H4O | C. | C2H4O2 | D. | C3H8O |
18.有机物M可用于合成香料,其结构简式如图所示.下列有关说法不正确的是( )
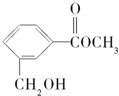

| A. | 有机物M中有2种含氧官能团 | |
| B. | 1mol有机物M可与1mol NaOH发生反应 | |
| C. | 有机物M能与溴水发生加成反应 | |
| D. | 1mol有机物M最多能与3mol H2反应 |