题目内容
9.配制0.10mol/L的NaOH溶液,下列操作会导致所配的溶液浓度偏高的是( )| A. | 用敞口容器称量NaOH且时间过长 | |
| B. | 定容时俯视读取刻度 | |
| C. | 原容量瓶洗净后未干燥 | |
| D. | 配制过程中,未用蒸馏水洗涤烧杯和玻璃棒 |
分析 分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析,凡是使n偏大,V偏小的操作都能使溶液浓度偏高,反之溶液浓度偏低,据此分析解答.
解答 解:A.用敞口容器称量NaOH且时间过长,导致称取的溶质中含有氢氧化钠的质量偏小,溶质的物质的量偏小,溶液浓度偏低,故A不选;
B.定容时俯视读取刻度,导致溶液体积偏小,溶液浓度偏高,故B选;
C.原容量瓶洗净后未干燥,对溶液体积、溶质的物质的量都不会产生影响,溶液浓度不变,故C不选;
D.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,溶液浓度偏低,故D不选;
故选:B.
点评 本题考查了一定物质的量浓度溶液的配制误差分析,准确分析操作对溶质的物质的量和溶液体积的影响是解题关键,题目难度不大.

练习册系列答案
相关题目
19.在2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O反应中氧化剂与氧化产物物质的量之比为( )
| A. | 1:8 | B. | 8:1 | C. | 2:5 | D. | 5:2 |
20.下列各组物质,前者属于电解质,后者属于非电解质的是( )
| A. | NaCl晶体、BaSO4 | B. | 铜、二氧化硫 | C. | 硫酸溶液、HCl | D. | 熔融的KNO3、酒精 |
17.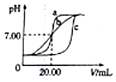 某班学生用0.1mol•L-1盐酸和0.1mol•L-1NaOH溶液反应测定酸碱滴定曲线,甲、乙、丙三组同学锥形瓶中的溶液所取体积均为20.00mL,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示,下列说法错误的是( )
某班学生用0.1mol•L-1盐酸和0.1mol•L-1NaOH溶液反应测定酸碱滴定曲线,甲、乙、丙三组同学锥形瓶中的溶液所取体积均为20.00mL,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示,下列说法错误的是( )
 某班学生用0.1mol•L-1盐酸和0.1mol•L-1NaOH溶液反应测定酸碱滴定曲线,甲、乙、丙三组同学锥形瓶中的溶液所取体积均为20.00mL,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示,下列说法错误的是( )
某班学生用0.1mol•L-1盐酸和0.1mol•L-1NaOH溶液反应测定酸碱滴定曲线,甲、乙、丙三组同学锥形瓶中的溶液所取体积均为20.00mL,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示,下列说法错误的是( )| A. | 乙组同学操作上的不足是在滴定终点附近测试和记录pH的间隔太大 | |
| B. | 甲组同学滴定时选用的滴定管为酸式滴定管 | |
| C. | 乙和丙两组同学的操作均存在不足或失误 | |
| D. | 丙组同学可能是用待测液润洗了锥形瓶 |
4.在溶液导电性实验中,往氢氧化钡溶液中滴加硫酸至过量,灯泡的明亮度变化是:明→暗→明,下列说法正确的是( )
| A. | 溶液的导电性与溶液中离子的浓度有关 | |
| B. | 溶液的导电性与溶液中离子数目的多少有关 | |
| C. | 恰好完全反应时,溶液不易导电,所以BaSO4和水都是非电解质 | |
| D. | 往氢氧化钡溶液中滴加盐酸与滴加硫酸时现象相同 |
14.某烷烃只能生成一种一氯化物,此烷烃的分子式不可能是( )
| A. | CH4 | B. | C4H10 | C. | C5H12 | D. | C8H18 |
3.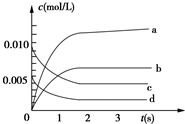 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
(1)800℃,反应达到平衡时,NO的物质的量浓度是0.0035mol/L;
(2)如图中表示NO2的变化的曲线是b.用O2表示从0~2s内该反应的平均速率v=1.5×10-3 mol/(L•s).
(3)能说明该反应已达到平衡状态的是b、c.
a.v(NO2)=2v(O2)b.容器内压强保持不变
c.v逆(NO)=2v正(O2)d.容器内密度保持不变
(4)能使该反应的反应速率增大的是bcd.
a.及时分离出NO2气体b.适当升高温度
c.增大O2的浓度d.选择高效催化剂.
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图中表示NO2的变化的曲线是b.用O2表示从0~2s内该反应的平均速率v=1.5×10-3 mol/(L•s).
(3)能说明该反应已达到平衡状态的是b、c.
a.v(NO2)=2v(O2)b.容器内压强保持不变
c.v逆(NO)=2v正(O2)d.容器内密度保持不变
(4)能使该反应的反应速率增大的是bcd.
a.及时分离出NO2气体b.适当升高温度
c.增大O2的浓度d.选择高效催化剂.
4.下列表述正确的是( )
| A. | 硫酸铝的电离方程式:Al2(SO4)3=2Al3++3SO42- | |
| B. | 小苏打的电离方程式:NaHCO3=Na++H++CO32- | |
| C. | Mg(OH)2难溶于水,所以Mg(OH)2不是电解质,而是非电解质 | |
| D. | K2CO3溶液能导电,所以K2CO3溶液是电解质 |