题目内容
100mL浓度为2mol/L的盐酸跟过量的锌片反应,为减慢反应速率,又不影响生成氢气的总量,可采用的方法是( )
| A、加入适量NaCl溶液 |
| B、加入适量NaOH溶液 |
| C、加入数滴CuCl2溶液 |
| D、加入适量NaNO3溶液 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:Zn过量,生成氢气由盐酸定,为了减慢反应速率,且不影响生成氢气的总量,可减小氢离子的浓度,但不能改变盐酸的物质的量,以此来解答.
解答:
解:A.加入适量NaCl溶液,溶液体积增大,反应速率减小,由于盐酸物质的量不变,则生成氢气的总量不变,故A正确;
B.加入适量NaOH溶液,消耗盐酸,生成氢气的总量减小,故B错误;
C.加入数滴CuCl2溶液,锌置换出铜,形成原电池反应,反应速率增大,故C错误;
D.加入适量NaNO3溶液,不能生成氢气,生成气体为NO,故D错误.
故选A.
B.加入适量NaOH溶液,消耗盐酸,生成氢气的总量减小,故B错误;
C.加入数滴CuCl2溶液,锌置换出铜,形成原电池反应,反应速率增大,故C错误;
D.加入适量NaNO3溶液,不能生成氢气,生成气体为NO,故D错误.
故选A.
点评:本题考查影响反应速率的因素,为高考常考考点,注意Zn过量,生成氢气由盐酸定,把握浓度、温度、原电池对反应速率的影响即可解答,题目难度不大.

练习册系列答案
相关题目
配制100mL 1.00mol/L NaCl 溶液,下列说法正确的是( )
| A、将所需量的NaCl溶于100mL水中 |
| B、将所需量的NaCl溶于少量水中,再加水定容到100mL |
| C、将所需量的NaCl直接放入容量瓶中,加水定容到100mL |
| D、定容时俯视读刻度 |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、1molNa+含有质子数为10NA |
| B、标况下,2.24升CCl4物质的量为0.1mol |
| C、标准状况下,分子数为NA的CO、N2混合气体体积约为22.4L,质量为28g |
| D、5.6g金属铁与足量盐酸反应时,失去0.3NA个电子 |
符合H++OH-=H2O这一离子方程式的是( )
| A、氢氧化铁和硫酸 |
| B、碳酸钠溶液与盐酸 |
| C、氢氧化铜与硝酸 |
| D、氢氧化钠和盐酸 |
下列叙述正确的是( )
| A、物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA |
| B、标准状况下,22.4 L O2和O3的混合气体所含分子数为NA |
| C、欲配置1.00L,1.00mol?L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 |
| D、2克氢气所含原子数约为6.02×1023 |
在NaCl、MgCl2、MgSO4三种盐配制的混合液中,Na+为0.2mol,Mg2+为0.25mol,Cl-为0.2mol,则SO42-为( )
| A、0.5 mol |
| B、0.15 mol |
| C、0.25 mol |
| D、0.2 mol |
下列与实验相关的叙述正确的是( )
| A、稀释浓硫酸时,应将蒸馏水沿烧杯内壁缓慢地注入浓硫酸中并不断搅拌 |
| B、配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
| C、配制1mol?L-1 300mL NaCl溶液可以选择一个50mL的容量瓶和一个250mL的容量瓶 |
D、可以用如图装置进行氯气的尾气处理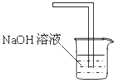 |
已知化学式为C4H10O的醇有4种异构体,若在该分子中增加1个羰基,形成的C5H10O2的羧酸可能有的结构有( )
| A、2种 | B、4种 | C、6种 | D、5种 |