题目内容
![]() 根据右表提供的数据,判断在等浓度的
根据右表提供的数据,判断在等浓度的![]() 、
、![]() 混合溶液中,各种离子浓度关系正确的是
混合溶液中,各种离子浓度关系正确的是
![]() A.
A.![]()
![]() B.
B.![]()
![]() C.
C.![]()
![]() D.
D.![]()
A
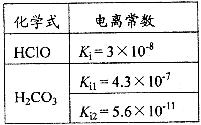
解析:
由表中数据可知HClO的酸性比H2CO3弱但是比HCO3- 强。
A、ClO-和HCO3—-都发生水解,由于越弱越水解,ClO-水解程度大,所以HCO3-浓度大于ClO-,所以A正确。
B、与A相反所以B错误。
C、这是个等式关系,所以应该找出这个等式建立的依据。从等式中可看到左侧都含Cl而右侧则都含C,所以可利用物料守恒知道左侧都是含Cl的所有微粒的浓度之和,而右侧则缺少CO32 -。因NaClO和NaHCO3浓度相同所以溶液中含Cl元素的微粒浓度之和等于所有含C元素的微粒浓度之和,故C错。
D、这依然是个等式关系,通过等式发现左侧都为阳离子而右侧都为阴离子,这显然是个电荷守恒的等式。进一步会发现右侧阴离子缺少CO32 -,所以等式不成立,D错。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 、
、 混合溶液中,各种离子浓度关系正确的是 ( )
混合溶液中,各种离子浓度关系正确的是 ( )






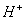 H+的能力:
H+的能力:


 、
、 混合溶液中,各种离子浓度关系正确的是
(
)
混合溶液中,各种离子浓度关系正确的是
(
)



