题目内容
14.铁的合金是当今世界使用量最大的合金,下列关于铁及其化合物的说法正确的是( )| A. | 铁的氧化物都具有磁性 | |
| B. | 氢氧化亚铁在空气中加热会分解生成氧化亚铁和水蒸气 | |
| C. | 铁在空气中放置表面会生成致密的氧化膜从而阻止铁被继续腐蚀 | |
| D. | 四氧化三铁可以通过置换反应或化合反应制备 |
分析 A、磁性氧化物为四氧化三铁;
B、氢氧化亚铁在空气中被氧化成氢氧化铁;
C、铁在空气中放置表面生成铁锈;
D、四氧化三铁可以由铁与氧气反应生成,也可以由铁与水蒸气反应制得.
解答 解:A、磁性氧化物为四氧化三铁,而不是氧化铁,故A错误;
B、氢氧化亚铁极易被氧化,所以氢氧化亚铁在空气中被氧化成氢氧化铁,而不是分解生成氧化亚铁和水蒸气,故B错误;
C、铁在空气中放置表面发生电化学腐蚀而生成铁锈,而不是生成致密的氧化膜,故C错误;
D、铁在氧气中燃烧生成四氧化三铁是化合反应;铁与水蒸气反应生成四氧化三铁和氢气是置换反应,所以四氧化三铁可以通过置换反应或化合反应制备,故D 正确;
故选D.
点评 本题考查铁的化合物的性质,难度不大,四氧化三铁的制取可以通过化合和置换的方法,掌握基础是关键.

练习册系列答案
相关题目
5.短周期元素A和B形成的化合物AB2有多种可能,对这些可能的化合物的判断正确的是( )
| A. | 化合物AB2不可能是离子化合物 | |
| B. | 化合物AB2的晶体可能是分子晶体、离子晶体或原子晶体 | |
| C. | 化合物AB2的熔点不可能很高 | |
| D. | 化合物AB2的空间立体结构不可能是V形结构 |
2.下列说法正确的是( )
| A. | 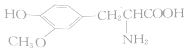 与 与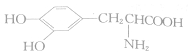 互为同系物 互为同系物 | |
| B. | CH3CH=CHCH3分子中所有原子在同一平面上 | |
| C. | 按系统命名法,化合物 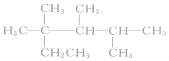 的名称是2,3,4-三甲基-2-乙基戊烷 的名称是2,3,4-三甲基-2-乙基戊烷 | |
| D. | 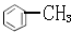 的一溴代物和 的一溴代物和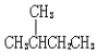 的一溴代物都有4种(不考虑立体结构) 的一溴代物都有4种(不考虑立体结构) |
9.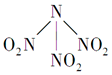 科学家最近研制出有望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )
科学家最近研制出有望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )
 科学家最近研制出有望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )
科学家最近研制出有望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )| A. | 分子中N、O间形成的共价键是非极性键 | |
| B. | 分子中4个氮原子共平面 | |
| C. | 该分子中的中心氮原子还有一对孤电子对 | |
| D. | 15.2 g该物质含有6.02×1022个原子 |
19.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ | |
| B. | 由水电离的c(H+)=1×10-14mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3- | |
| C. | c(Fe3+)=0.1 mol•L-1的溶液中:K+、ClO-、SO42-、SCN- | |
| D. | c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- |
6.氢化亚铜(CuH)是一种难溶物质,具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是:2Cu+═Cu2++Cu.根据以上信息,下列叙述正确的是( )
| A. | 用CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中作氧化剂 | |
| B. | CuH在氯气中燃烧的化学反应方程式为2CuH+3Cl2 $\frac{\underline{\;点燃\;}}{\;}$2CuCl2+2HCl | |
| C. | CuH溶解在稀盐酸中生成的气体是氯气 | |
| D. | 如果选项C反应中生成了标准状况下22.4 L的气体,则转移电子3 mol |
3.下列离子方程式中,错误的是( )
| A. | 氯气与烧碱溶液反应:Cl2+2OH-=Cl-+ClO-+H2O | |
| B. | 稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ | |
| C. | 二氧化硅与强碱反应:SiO2+2OH-═SiO32-+H2O | |
| D. | 二氧化氮与水反应:3NO2+H2O═2H++2NO3-+NO |
4.下列装置或操作正确并能达到实验目的( )
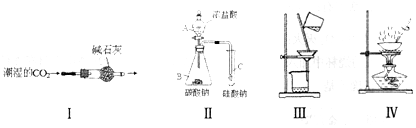

| A. | 用Ⅰ图装置,可得到干燥的CO2 | |
| B. | 用Ⅱ图装置,若C中出现白色沉淀,则可说明H2CO3的酸性强于H2SiO3 | |
| C. | 用Ⅲ图装置,可除去氯化钠溶液中的泥沙 | |
| D. | 用Ⅳ图装置,分离乙醇和水 |