题目内容
7.SO2、NO是大气污染物.吸收SO2 和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):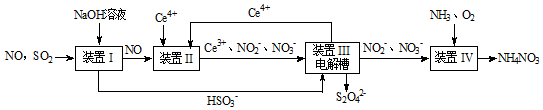
(1)装置Ⅰ中生成HSO3-的离子方程式为SO2+OH-=HSO3-.
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH 的关系如图1所示.
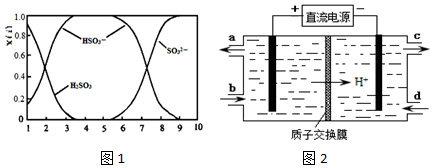
①下列说法正确的是ac (填字母序号).
a.pH=8时,溶液中c(HSO3-)<c(SO32-)
b.pH=7时,溶液中c(Na+)=c(HSO3-)+c(SO32-)
c.为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因:HSO3-在溶液中存在电离平衡:HSO3-?SO32-+H+,加CaCl2溶液后,Ca2++SO32-=CaSO3↓使电离平衡右移,c(H+)增大.
(3)装置Ⅱ中酸性条件下NO被Ce4+氧化的产物主要是NO3-、NO2-,写出生成NO3-时的离子方程式NO+2H2O+3Ce4+=3Ce3++NO3-+4H+.
(4)装置Ⅲ的作用之一是再生Ce4+,同时获得副产品Na2S2O4,其原理如图2所示.
①阴极的电极反应式为2HSO3-+4H++4e-=S2O32-+3H2O.
②生成Ce4+从电解槽的a(填字母序号)口流出.
(5)从氧化池Ⅳ中得到的粗产品NH4NO3的实验操作是蒸发浓缩、冷却结晶,过滤、洗涤等.标况下,若V L尾气(设气体体积分数:NO为a%、SO2为b%、CO2为c%)经上述流程变化后最终获得m g NH4NO3,则尾气中NO的利用率为$\frac{28m}{aV}$%.
分析 吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程分析可知,混合气体通入氢氧化钠溶液中吸收二氧化硫,剩余一氧化氮装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,进入装置Ⅲ电解再生Ce4+循环使用,最后剩余的NO3-、NO2-通入氨气和氧气反应得到硝酸铵,
(1)二氧化硫是酸性氧化物,能和强碱之间发生反应;
(2)①当溶液的pH=8时,根据图示得到溶液是亚硫酸钠和亚硫酸氢钠的混合物,根据离子浓度大小比较的方法来回答;
②NaHSO3溶液中HSO3-的电离大于水解,溶液显示酸性,根据平衡移动原理来回答;
(3)在酸性环境下,NO和Ce4+之间会发生氧化还原反应;
(4)在电解池中,阳极上发失去电子的氧化反应,阴极上发生得电子的还原反应;氮元素守恒计算;
(5)溶液中得到溶质固体的方法是蒸发浓缩、冷却结晶、过滤洗涤、干燥等,标况下,若V L尾气(设气体体积分数:NO为a%、SO2为b%、CO2为c%)经上述流程变化后最终获得m g NH4NO3,其中铵根来源于通入的氨气,硝酸根离子中的氮元素来源于混合气体中的一氧化氮,结合元素守恒计算得到.
解答 解:(1)二氧化硫是酸性氧化物,能和强碱氢氧化钠之间发生反应:SO2+OH-=HSO3-,故答案为:SO2+OH-=HSO3-;
(2)①a、当溶液的pH=8时,根据图示得到溶液是亚硫酸钠和亚硫酸氢钠的混合物,离子浓度大小顺序是:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+),c(SO32-)>c(HSO3-),故a正确;
b.pH=7时,溶液呈中性,c(H+)=c(OH-),溶液中存在电荷守恒:c(H+)+c(Na+)=c(HSO3-)+2c(SO32-)+c(OH-),故溶液中c(Na+)=c(HSO3-)+2c(SO32-),故b错误;
c.图象可知,为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右.故c正确;
故答案为:ac;
②NaHSO3溶液中HSO3-的电离大于水解,HSO3-?SO32-+H+,溶液显示酸性,加入CaCl2溶液后,Ca2++SO32-=CaSO3↓使电离平衡右移,
故答案为:HSO3-在溶液中存在电离平衡:HSO3-?SO32-+H+,加CaCl2溶液后,Ca2++SO32-=CaSO3↓使电离平衡右移,c(H+)增大;
(3)在酸性环境下,NO和Ce4+之间会发生氧化还原反应:NO+2H2O+3Ce4+=3Ce3++NO3-+4H+,
故答案为:NO+2H2O+3Ce4+=3Ce3++NO3-+4H+;
(4)①电解池的阴极发生得电子的还原反应,电极反应式为:2HSO3-+4H++4e-=S2O32-+3H2O,阳极电极反应为:Ce3+-e-═Ce4+,
故答案为:2HSO3-+4H++4e-=S2O32-+3H2O;
②在电解池中,阳极上是Ce3+失电子成为Ce4+的过程,所以生成Ce4+从电解槽的阳极上极a极流出,
故答案为:a;
(5)在氧化池Ⅵ中得到NH4NO3溶液,从NH4NO3溶液中得到硝酸铵可以通过蒸发浓缩,冷却结晶、过滤、洗涤等操作获得,标况下,若V L尾气(设气体体积分数:NO为a%、SO2为b%、CO2为c%)经上述流程变化后最终获得m g NH4NO3,尾气中NO最后变化为硝酸根离子,则尾气中NO的利用率=$\frac{\frac{mg}{80g/mol}}{\frac{Va%L}{22.4L/mol}}$×100%=$\frac{28m}{aV}$%,
故答案为:蒸发浓缩、冷却结晶;$\frac{28m}{aV}$%.
点评 本题综合考查学生含氮元素、含硫元素物质的性质知识,注意知识的梳理和归纳是关键,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 1molH2燃烧放出的热量为H2的燃烧热 | |
| B. | 某吸热反应能自发进行,因此该反应是熵增反应 | |
| C. | 向饱和硼酸溶液中滴加Na2CO3溶液,有CO2气体生成 | |
| D. | 原电池中发生的反应达平衡时,该电池仍有电流产生 |
 某条件下,在2L密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.下列有关说法不正确的是( )
某条件下,在2L密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.下列有关说法不正确的是( )| A. | 反应2min末X的浓度为0.35mol/L | |
| B. | 该反应的化学方程式可表示为:2Z?2Y+3X | |
| C. | 反应2min内以Z浓度变化表示的平均反应速率为0.05mol/(L•min) | |
| D. | 任何时刻以Z、Y浓度变化表示的反应速率关系符合υ(Z)=υ(Y) |
| 甲 | 乙 | 丙 | 丁 | ||
| 密闭容器体积/L | 2 | 2 | 2 | 1 | |
| 起始物质的量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 | 0.4 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
| SO2的平衡转化率/% | 80 | a1 | a2 | a3 | |
| A. | 该温度下,该反应的平衡常数K为400 | |
| B. | SO2的平衡转化率:a1>a2=a3 | |
| C. | 达到平衡时,容器丁中的正反应速率比容器丙中的大 | |
| D. | 达到平衡时,容器丙中c( SO3)大于容器甲中c( SO3)的两倍 |
| A. | 0.1mol•L-1NaHC2O4溶液(pH=5.5):c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-) | |
| B. | 0.1mol•L-1NaHS溶液:c(OH-)+c(S2-)═c(H+)+c(H2S) | |
| C. | 0.1mol•L-1CH3COOH溶液和0.1mol•L-1CH3COONa溶液等体积混合:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
| 物质性质 | 实际应用 | |
| A | 硅胶吸水能力强 | 食品、药品干燥剂 |
| B | 油脂在碱性条件下水解 | 制肥皂 |
| C | SiO2是酸性氧化物 | 光导纤维 |
| D | Na2O2与CO2、H2O反应 | 潜水艇中作为氧气来源 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 原子半径:Y>Z>W>X | |
| B. | 气态氢化物的热稳定性:X>W | |
| C. | 工业上常用电解对应氯化物的方法制备单质 Z | |
| D. | Y 的最高价氧化物对应的水化物可溶于氯化铵溶液 |