题目内容
A、B、C、D四种短周期元素的原子半径依次减小,A与C核电荷数之比为3:4,D能分别与A、B、C形成电子总数相等的分子X、Y、Z.下列叙述正确的是( )
| A、X、Y、Z的稳定性逐渐减弱 |
| B、A、B、C、D只能形成5种单质 |
| C、X、Y、Z三种化合物的熔、沸点逐渐升高 |
| D、由A、B、C、D四种元素既能组成共价化合物又能组成离子化合物 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:A、B、C、D四种短周期元素的原子半径依次减小,A与C核电荷数之比为3:4,A、C只能为同周期元素,两元素有Li和Be、C和O、Mg和S,D能分别与A、B、C形成电子总数相等的分子X、Y、Z,考虑10电子微粒,可推知A为C元素,C为O元素,D为H元素,则B为N元素,X、Y、Z分别为CH4、NH3、H2O,结合元素周期律及物质性质解答.
解答:
解:A、B、C、D四种短周期元素的原子半径依次减小,A与C核电荷数之比为3:4的两元素有Li和Be、C和O、F和Mg、Mg和S,D能分别与A、B、C形成电子总数相等的分子X、Y、Z.A为C元素,C为O元素,D为H元素,则B为N元素.X、Y、Z分别为CH4、NH3、H2O.
A.非金属性越强,氢化物越稳定,同周期随原子序数增大,非金属性增强,所以非金属性C<N<O,所以CH4、NH3、H2O的稳定性逐渐增强,故A错误;
B.由于C元素有非常多的同素异形体金刚石、石墨、C60、C70、C100等,氧元素只存在O2、O3等,故B错误;
C.NH3分子间形成氢键比CH4分子间作用力大,沸点高,水常温是液体,沸点最高,所以X、Y、Z三种化合物的熔、沸点逐渐升高,故C正确;
D.四元素组成的化合物除常见的碳酸铵、碳酸氢铵外,有机物中硝基化合物、硝酸酯、氨基酸、蛋白质等均属于C、H、O、N组成的化合物,则既能组成共价化合物又能组成离子化合物,故D正确.
故选:CD.
A.非金属性越强,氢化物越稳定,同周期随原子序数增大,非金属性增强,所以非金属性C<N<O,所以CH4、NH3、H2O的稳定性逐渐增强,故A错误;
B.由于C元素有非常多的同素异形体金刚石、石墨、C60、C70、C100等,氧元素只存在O2、O3等,故B错误;
C.NH3分子间形成氢键比CH4分子间作用力大,沸点高,水常温是液体,沸点最高,所以X、Y、Z三种化合物的熔、沸点逐渐升高,故C正确;
D.四元素组成的化合物除常见的碳酸铵、碳酸氢铵外,有机物中硝基化合物、硝酸酯、氨基酸、蛋白质等均属于C、H、O、N组成的化合物,则既能组成共价化合物又能组成离子化合物,故D正确.
故选:CD.
点评:本题考查原子结构、元素周期律的有关知识,为高频考点,侧重于学生的分析能力的考查,难度中等,推断元素是解题关键,A、C核电荷数关系是突破口,D选项中注意考虑有机物.

练习册系列答案
 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
往CuO和Fe粉的混合物中,加入一定量的稀硫酸,并微热,当反应停止后,滤出不溶物,并向滤液中插入一枚光亮的铁钉,片刻后,取出铁钉,发现铁钉无任何变化.根据上述现象,确定下面结论正确的是( )
| A、滤出的不溶物一定是铜 |
| B、滤出的不溶物一定含铜,但不一定含铁 |
| C、滤出的不溶物一定是铁 |
| D、滤液中一定含有Fe2+和Cu2+ |
在1L的密闭容器中,于一定温度下进行2A(g)+B(g)?2C(g)的可逆反应.容器内开始加入下列各组物质,在达到平衡时逆反应速率最大的一组物质是( )
| A、2molA 1molB |
| B、1molA 1molB |
| C、1molA 2molB |
| D、1molB 1molC |
下列反应中,以苯作原料,通过加成反应制得的是( )
| A、溴苯 | B、硝基苯 |
| C、苯磺酸 | D、环己烷 |
 已知25℃时有关弱酸的电离平衡常数:
已知25℃时有关弱酸的电离平衡常数:
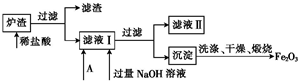
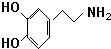
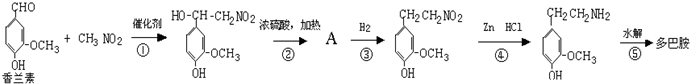 (3)多巴胺可由香兰素与硝基甲烷缩合,再经锌-盐酸还原水解而得.合成过程表示如下:
(3)多巴胺可由香兰素与硝基甲烷缩合,再经锌-盐酸还原水解而得.合成过程表示如下: