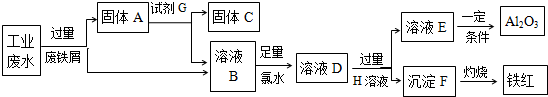
题目内容
11.海洋植物如海带海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海洋植物海藻中提取碘的流程如下: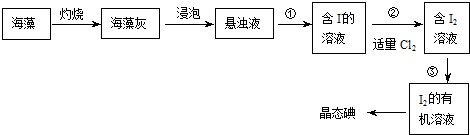
(1)指出提取的过程中有关实验操作名称:①过滤、③萃取、分液.
(2)提取碘的过程中,操作③可以选用的有机溶剂是BD.(填字母)
(A)水 (B)四氯化碳 (C)酒精 (D)苯
操作③在实验室中需要用到的玻璃仪器有分液漏斗、烧杯
(3)写出过程②的化学方程式(I-以碘化钾为例),并分析电子转移的方向和数目.
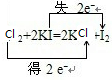
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏操作.
分析 从海带中提取碘:海带灼烧后得到海带灰浸泡后得到海带灰的浊液,将悬浊液分离为残渣和含碘离子溶液应选择过滤的方法,过滤得到含碘离子的溶液加入Cl2可氧化碘离子为碘单质,得到含碘水溶液,加入有机溶剂苯或四氯化碳,萃取分液得到含碘的苯或四氯化碳溶液,通过蒸馏得到碘单质.
(1)分离固体和液体用过滤,利用溶解性的差异来分析;
(2)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,萃取剂与溶质不反应,据此来选择合适的试剂和玻璃仪器;
(3)化合价降低元素所在的反应物是氧化剂,化合价升高元素所在的反应物是还原剂,反应中,化合价升高数目=化合价降低数目=转移电子数目;
(4)从含碘的有机溶液中提取碘和回收有机溶剂还需经过蒸馏.
解答 解:(1)过滤适用于不溶于水的固体和液体,分离固体和液体用过滤;将碘水中的碘单质萃取出来,选择合适的萃取剂即可,
故答案为:过滤;萃取;
(2)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,萃取剂与溶质不反应,碘在四氯化碳或苯中的溶解度大于在水中的溶解度,四氯化碳或苯和水都不互溶,且四氯化碳或苯和碘都不反应,故可用四氯化碳或苯,萃取需要用到的玻璃仪器有分液漏斗、烧杯,
故答案为:BD;分液漏斗、烧杯;
(3)反应Cl2+2KI=2KCl+I2中,化合价降低的元素是氯元素,得到电子,所以Cl2是氧化剂,化合价升高元素是碘元素,失电子,化合价升高数目=化合价降低数目=转移电子数目=2,电子转移的方向和数目如下所示: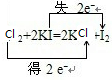 ,
,
故答案为: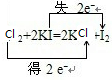 Br2;
Br2;
(4)从有机溶剂中提取碘,需要用蒸馏操作,
故答案为:蒸馏.
点评 本题考查了海水资源及其综合运用,侧重从海带中提取碘,涉及物质的分离、检验、仪器的选取等知识点,根据物质的特点及性质选取相应的分离和检验方法,根据仪器的作用选取仪器,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 甲烷 | B. | 乙烯 | C. | 苯 | D. | 乙炔 |
| A | ||||
| E | B | C | D |
(2)A与氢元素能形成原子物质的量之比为1:1的化合物,其化学式为H2O2;
(3)C的最高价氧化物的水化物与E单质的反应属于放热反应(填“吸热”或“放热”);生成物的总能量小于(填“大于”、“小于”或“等于”)反应物的总能量.
| A. | Cs与U的质子数差值为37 | B. | Cs与U的中子数差值为98 | ||
| C. | 铯137的电子数是82 | D. | 铀元素的相对原子质量是235 |
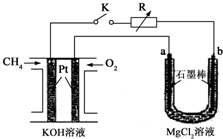 新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源进行氯化镁溶液电解实验,电解装置如图所示.请回答下列问题:
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源进行氯化镁溶液电解实验,电解装置如图所示.请回答下列问题: