题目内容
2KMnO4+16HCl═2MnCl2+5Cl2↑+8H2O+2KCl,在这个反应中,氧化剂是 ,氧化产物是 ,用双线桥标出电子的转移方向和数目 .
考点:氧化还原反应
专题:氧化还原反应专题
分析:2KMnO4+16HCl═2MnCl2+5Cl2↑+8H2O+2KCl中,Mn元素的化合价降低,Cl元素的化合价升高,该反应转移10e-,以此来解答.
解答:
解:2KMnO4+16HCl═2MnCl2+5Cl2↑+8H2O+2KCl中,Mn元素的化合价降低,KMnO4为氧化剂,Cl元素的化合价升高,被氧化,则氧化产物为Cl2,该反应转移10e-,双线桥标出电子的转移方向和数目为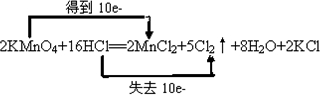 ,
,
故答案为:KMnO4;Cl2; .
.
 ,
,故答案为:KMnO4;Cl2;
 .
.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重电子的转移、氧化剂和还原剂的判断的考查,注意从化合价角度分析,难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
下列说法正确的是( )
| A、含有离子键的化合物一定是离子化合物,在离子化合物中可以含有非极性共价键 |
| B、含有共价键的化合物一定是共价化合物,在共价化合物中一定含有共价键 |
| C、非极性共价键只能存在于非金属单质中,不可能存在于化合物中 |
| D、不同元素原子形成的多原子分子中,含有的化学键只能是极性共价键 |
根据共价键成键特点:1个C有4个未成键电子,1个O有2个未成键电子,1个H有1个未成键电子,1个N有3个未成键电子,4位同学据此分别提出以下4种该有机物可能的分子式,其中合理的是( )
| A、C2H5 |
| B、C4H12O |
| C、C7H10NO2 |
| D、C6H10O4 |



