题目内容
水的电离平衡曲线如图所示,下列说法不正确的是( )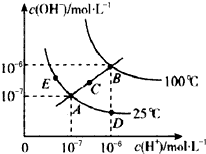

| A、图中五点KW间的关系:B>C>A=D=E |
| B、若从A点到D点,可采用:温度不变在水中加入少量的酸 |
| C、若处在B点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性 |
| D、若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl固体 |
考点:电解质在水溶液中的电离
专题:电离平衡与溶液的pH专题
分析:A、ADE都处于250C时,Kw相等,然后比较B、E两点的c(H+)和c(OH-)的大小,依次比较Kw的大小;
B、从A点到D点c(H+)变大,但c(OH-)变小,温度不变,Kw不变;
C、根据B点时Kw计算酸与碱溶液中c(H+)和c(OH-),然后判断溶液的酸碱性;
D、从A点到C点c(H+)和c(OH-)的变化判断Kw的变化,依次判断温度的变化.
B、从A点到D点c(H+)变大,但c(OH-)变小,温度不变,Kw不变;
C、根据B点时Kw计算酸与碱溶液中c(H+)和c(OH-),然后判断溶液的酸碱性;
D、从A点到C点c(H+)和c(OH-)的变化判断Kw的变化,依次判断温度的变化.
解答:
解:A、ADE都处于250C时,Kw相等,B点c(H+)和c(OH-)都大于E点的c(H+)和c(OH-),并且C点的c(H+)和c(OH-)大于A点c(H+)和c(OH-),c(H+)和c(OH-)越大,Kw越大,故B>C>A=D=E,故A正确;
B、加酸,c(H+)变大,但c(OH-)变小,但温度不变,Kw不变,故B正确;
C、若处在B点时,Kw=1×10-12,pH=2的硫酸中c(H+)=10-2mol/L,pH=10的KOH中c(OH-)=10-2mol?L-1,等体积混合,恰好中和,溶液显中性,故C正确;
D、若从A点到C点,c(H+)变大,c(OH-)变大,Kw增大,温度应升高,加入适量的NH4Cl固体Kw不变,故D错误;
故选D.
B、加酸,c(H+)变大,但c(OH-)变小,但温度不变,Kw不变,故B正确;
C、若处在B点时,Kw=1×10-12,pH=2的硫酸中c(H+)=10-2mol/L,pH=10的KOH中c(OH-)=10-2mol?L-1,等体积混合,恰好中和,溶液显中性,故C正确;
D、若从A点到C点,c(H+)变大,c(OH-)变大,Kw增大,温度应升高,加入适量的NH4Cl固体Kw不变,故D错误;
故选D.
点评:本题考查水的电离平衡移动问题,结合图象判断并分析溶液在不同温度下的Kw,做题时注意根据图象比较c(H+)和c(OH-)的大小.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用Pauling的杂化轨道理论解释甲烷分子的四面体结构,下列说法不正确的是( )
| A、C原子的四个杂化轨道的能量一样 |
| B、C原子的sp3杂化轨道之间夹角一样 |
| C、C原子的4个价电子分别占据4个sp3杂化轨道 |
| D、C原子有1个sp3杂化轨道由孤对电子占据 |
下列对有机物结构或性质的描述,错误的是( )
| A、一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应 |
| B、苯和乙烯,只有乙烯能与H2发生加成反应 |
| C、乙烷和丙烯的物质的量共1 mol,完全燃烧生成3 mol H2O |
| D、光照下2,2-二甲基丙烷与Br2反应,其一溴取代物只有一种 |
下列物质的说法不正确的是( )
| A、天然气的主要成份是乙烯,芳香烃主要来自于煤的干馏后的煤焦油 |
| B、研究有机物一般要经过的基本步骤为:分离、提纯→元素定量分析(确定实验式)→测定相对分子质量(确定分子式)→波谱分析(确定结构式),其中最早提出元素定量分析的是德国化学家李比希 |
| C、汽油、煤油、柴油主要来自于石油的常压蒸馏和石油的催化裂化 |
| D、甲烷、乙烷、丙烷中的化学键既有极性键又有非极性键 |
 把镁条投入到盛有盐酸的敞口容器里,产生H2的速率如图所示,在下列因素中,影响O~t1时间段反应速率的主要因素是( )
把镁条投入到盛有盐酸的敞口容器里,产生H2的速率如图所示,在下列因素中,影响O~t1时间段反应速率的主要因素是( )| A、盐酸的浓度 |
| B、镁条的表面积 |
| C、Cl-的浓度 |
| D、溶液的温度 |
判断下列有关化学基本概念的依据正确的是( )
| A、酸:电离产生的阳离子是否全部是氢离子 |
| B、化学平衡状态:正逆反应的反应速率是否等于0 |
| C、共价化合物:组成物质的元素是否全部是非金属元素 |
| D、化学变化:是否有热效应、颜色变化、气体或沉淀生成等实验现象 |
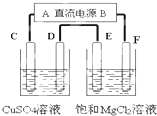 如图所示的装置,C、D、E、F都是惰性电极.将电源接通后,向1mol/L的MgCl2溶液中滴入酚酞溶液,在F极附近显红色.则以下说法正确的是( )
如图所示的装置,C、D、E、F都是惰性电极.将电源接通后,向1mol/L的MgCl2溶液中滴入酚酞溶液,在F极附近显红色.则以下说法正确的是( )| A、电源A极是负极 |
| B、左烧杯内溶液的pH减小,右烧杯有白色浑浊出现 |
| C、电极D是阳极,发生的电极反应为:4OH-+4e-═2H2O+O2 |
| D、C﹑D﹑E﹑F电极均有单质生成,其物质的量之比为2:1:1:1 |