题目内容
17.随着原子序数的递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图1所示: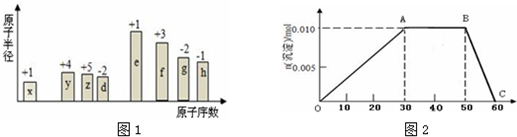
(1)h的原子结构示意图
 .
.(2)上述元素组成的复盐 (zx4) af b(gd4)c,向盛有10mL1mol•L-1该盐溶液中慢慢滴加1mol•L-1NaOH溶液,沉淀的物质的量随NaOH溶液体积变化如图2:
①a:b:c=4:2:5.
②图中AB段发生反应的离子方程式为NH4++OH-=NH3•H2O.
分析 从图中的化合价、原子半径的大小及原子序数,可知x是H元素,y是C元素,z是N元素,d是O元素,e是Na元素,f是Al元素,g是S元素,h是Cl元素.
(1)h为Cl元素,其原子核外有17个电子分三层排布;
(2)①R是(NH4) aAl b(SO4)c,根据Al3+、NH4+消耗的氢氧化钠计算ab,根据化合价的代数和为零计算c;
②m点过程中加入氢氧化钠,沉淀物质的量不变,是NH4+与OH-反应生成NH3•H2O.
解答 解:从图中的化合价、原子半径的大小及原子序数,可知x是H元素,y是C元素,z是N元素,d是O元素,e是Na元素,f是Al元素,g是S元素,h是Cl元素.
(1)h为Cl元素,其原子核外有17个电子分三层排布,其原子结构示意图为 ,故答案为:
,故答案为: ;
;
(2)①R是(NH4) aAl b(SO4)c,滴加氢氧化钠发生反应Al3++3OH-=Al(OH)3↓、NH4++OH-=NH3•H2O,根据消耗的氢氧化钠可知n(NH4+):n(Al3+)=2:1,当a=4,b=2时,由化合价的代数和为零可知,c=5,所以a:b:c=4:2:5,
故答案为:4:2:5;
②m点过程中加入氢氧化钠,沉淀物质的量不变,是NH4+与OH-反应生成NH3•H2O,离子方程式为:NH4++OH-=NH3•H2O,
故答案为:NH4++OH-=NH3•H2O.
点评 本题考查结构位置性质关系、化学图象及化学计算,是对学生综合能力的考查,需要学生具备扎实的基础,难度中等,注意把握图象中各段发生的反应.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
15.某饱和一元醇的结构简式如下,其系统命名是( )


| A. | 2,2-二甲基戊醇 | B. | 2,2-二甲基-4-戊醇 | ||
| C. | 1,3,3-三甲基丁醇 | D. | 4,4-二甲基-2-戊醇 |
8.常温下,部分弱酸的电离平衡常数如下表:
下列选项错误的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K1=1.76×10-5 | K1=4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | 中和等体积、等pH的CH3COOH溶液和HCN溶液消耗NaOH的量前者大于后者 | |
| B. | 可发生反应:2CH3COOH+CO32-=2CH3COO-+H2O+CO2↑ | |
| C. | Na+、CN-、CH3COO-、HCO3-等离子能大量共存 | |
| D. | 等浓度的CH3COONa和NaCN溶液pH前者小于后者 |
5.部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如下处理:

下列说法正确的是( )

下列说法正确的是( )
| A. | 样品中Fe元素的质量为2.24 g | B. | 滤液A中的阳离子为Fe2+、Fe3+、H+ | ||
| C. | 样品中CuO的质量为4.0 g | D. | V=896 |
2.在标准状况下,0.44g某气体的体积为224mL,则该气体的相对分子质量是( )
| A. | 2 | B. | 88 | C. | 44 | D. | 0.044 |
9.下列各组离子反应可用H++OH-=H2O表示的是( )
| A. | Cu(OH)2与H2SO4 | B. | Ba(OH)2与H2SO4 | C. | Fe(OH)3与HCl | D. | HNO3与KOH |
6.根据表中信息,判断下列叙述中正确的是( )
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | Cl- | |
| ② | KClO3 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| A. | 表中①组反应当n(FeBr2):n(Cl2)≥$\frac{1}{2}$一种元素被氧化、当n(FeBr2):n(Cl2)<$\frac{1}{2}$两种元素被氧化 | |
| B. | 氧化性强弱的比较:KClO3>Fe3+>Cl2>Br2 | |
| C. | 表中②组反应的还原产物是KCl,电子转移数目是6e- | |
| D. | 表中③组反应的离子方程式为:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O |
 ;
;