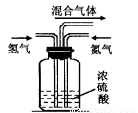
��Ŀ����
��12�֣���I��������������������ͭ��Cu2O�����Ǻ�ɫ��ĩ�����������ϡ���֪������ͭ����ϡ��������Cu��CuSO4��ijУ��ѧʵ��С��Ϊ��̽����Fe2O3��Cu2O��ɵĻ�������������ʵ�����Դ�С��ijͬѧ��ΪֻҪȡ������ĩ��������ϡ�����У�ͨ���۲����ɡ�
��1������ʵ������з����ķ�Ӧ�У������ӷ���ʽ��ʾ����
��Fe2O3+6H+= 2Fe3++3H2O
�� ��
��2����ʵ���й۲쵽��Һ��Ϊ��ɫ���й���ʣ�࣬��n��Cu2O�� n��Fe2O3�������>������<����=������
��II���ֱ����ܱ�������������Ӧ���н������·�Ӧ��
��Ӧ�ң�A��g��+2B��g��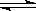 2C��g��
2C��g��
�ҷ�Ӧ�ң�2Z��g��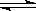 X��g��+Y��g��
X��g��+Y��g��
�ڷ�Ӧ��֮������Ħ���������ɻ������ܷ����ϡ���Ӧ��ʼ�ʹﵽƽ��ʱ�й��������ı仯����ͼ��ʾ��

��1��A��g��+2B��g�� 2C��g�� �ġ�H 0���>������<����=������
2C��g�� �ġ�H 0���>������<����=������
��2����ƽ�⣨I����ƽ�⣨���У�X��������� ������ţ���
a��һ����� b��һ������� c���������
��3���ﵽƽ�⣨I��ʱ��A��ת����Ϊ ��
��1��Cu2O+2H+=Cu+Cu2++H2O��Cu+2Fe3+=2Fe2++Cu2+����2��>
��(1) < (2) b (3) 5/11
��������
�����������1����Fe2O3��Cu2O��ɵĻ�����������ϡ�����з�ˮ��Ӧ�������������ᷴӦ��������ͭ��ˮ��������ͭ�����ᷴӦ����ͭ������ͭ��ˮ�����ɵ�ͭ����������Ӧ������������������ͭ����Ӧ���ӷ���ʽ����ΪFe2O3+6H+=2Fe3++3H2O��Cu2O+2H+=Cu+Cu2++H2O��Cu+2Fe3+=2Fe2++Cu2+��
����Cu2O+2H+=Cu+Cu2++H2O��Cu+2Fe3+=2Fe2++Cu2+��
��2����ʵ���й۲쵽��Һ��Ϊ��ɫ���й���ʣ�࣬˵��ͭ��ʣ�࣬��Һ����������ȫת��Ϊ������������Cu+2Fe3+=2Fe2++Cu2+��֪n��Cu����2n��Fe3+������Fe2O3+6H+=2Fe3++3H2O��֪n��Fe3+��=2n��Fe2O3������Cu2O+2H+=Cu+Cu2++H2O��֪n��Cu��=n��Cu2O������n��Cu2O����2n��Fe2O3������Ϊ������
II��1�����ҵĻ���������ʵ������䣬ƽ�⣨I����ƽ�⣨���������ҵ��¶ȡ�ѹǿ��ͬ�����֮�ȵ������ʵ���֮�ȣ���ͼ��֪��ƽ�⣨I�������¶ȴ���ƽ��ƽ�⣨��������2.8������2.6�������ҵ���������ʵ�����С�������¶�ƽ��������Ӧ�ƶ��������¶�ƽ������ȷ�Ӧ�ƶ����ʸ÷�Ӧ����ӦΪ���ȷ�Ӧ������H��0����Ϊ������
��2�������¶ȣ����ҵ�ƽ��һ���ƶ��������ܵ����ʵ������䣬X�ĺ���һ���仯��ƽ�⣨I����ƽ�⣨���У�X���������һ������ȣ�ѡ��b��
��3�����ҵĻ���������ʵ�������Ϊ2mol���������ҵ�ѹǿ���¶���ȣ�ͬ��ͬѹ�£����֮�ȵ������ʵ���֮�ȣ�ƽ�⣨I�������һ�������ܵ����ʵ���Ϊ2.8/2.2��2mol=28/11mol����μӷ�Ӧ��A�����ʵ���Ϊamol����
A��g��+2B��g�� 2C��g�����ʵ������١�n
2C��g�����ʵ������١�n
1 1
amol 3mol-28/11mol=5/11mol,���a=5/11mol,����A��ת����Ϊ(5��11)/1=5/11����Ϊ��5/11��
���㣺����ͭ�������仯��������ʣ�Ӱ�컯ѧƽ������ء�

 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д�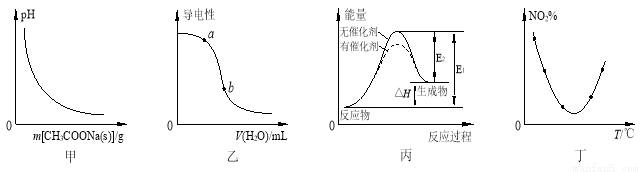
 N2O4(g)����ͬʱ�����NO2���������ߣ���÷�Ӧ�ġ�H��0
N2O4(g)����ͬʱ�����NO2���������ߣ���÷�Ӧ�ġ�H��0 NH4++NH2���������ӻ�����Ϊl��0xl0��30���ֽ�2��3g������Ͷ��1��0 LҺ���У���Һ������ƽ��____ �ƶ���������������������淽��������Ӧ����������Һ��������䣬������Һ��NH4+��Ũ��Ϊ____ ��
NH4++NH2���������ӻ�����Ϊl��0xl0��30���ֽ�2��3g������Ͷ��1��0 LҺ���У���Һ������ƽ��____ �ƶ���������������������淽��������Ӧ����������Һ��������䣬������Һ��NH4+��Ũ��Ϊ____ ��