题目内容
下列离子方程式表达正确的是( )
| A、漂白粉溶液中通入过量的CO2:ClO-+CO2+H2O=HClO+HCO3- | ||||
| B、用碳酸钠溶液吸收Br2:CO32-+Br2+2H2O=Br-+BrO3-+CO2↑+4H+ | ||||
C、用铜电极电解硫酸铜溶液:2Cu2++2H2O
| ||||
| D、已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液中,形成无色溶液,当在Pb(Ac)2醋酸铅溶液中通入H2S时,有黑色沉淀PbS生成:Pb2++2Ac-+H2S=PbS+2HAc |
考点:离子方程式的书写
专题:离子反应专题
分析:A.反应生成碳酸氢钙和HClO;
B.电子、电荷不守恒;
C.用铜电极电解硫酸铜溶液,阳极Cu失去电子,阴极铜离子得到电子;
D.Pb(Ac)2在离子反应中应保留化学式.
B.电子、电荷不守恒;
C.用铜电极电解硫酸铜溶液,阳极Cu失去电子,阴极铜离子得到电子;
D.Pb(Ac)2在离子反应中应保留化学式.
解答:
解:A.漂白粉溶液中通入过量的CO2的离子反应为ClO-+CO2+H2O=HClO+HCO3-,故A正确;
B.用碳酸钠溶液吸收Br2的离子反应为3Br2+6CO32-+3H2O=5Br-+BrO3-+6HCO3-,故B错误;
C.用铜电极电解硫酸铜溶液,阳极发生Cu-2e-=Cu2+,阴极发生Cu2++2e-=Cu,故C错误;
D.Pb(Ac)2溶液中通入H2S时有黑色沉淀生成,发生的离子反应为Pb(Ac)2+H2S=PbS↓+2HAc,故D错误;
故选A.
B.用碳酸钠溶液吸收Br2的离子反应为3Br2+6CO32-+3H2O=5Br-+BrO3-+6HCO3-,故B错误;
C.用铜电极电解硫酸铜溶液,阳极发生Cu-2e-=Cu2+,阴极发生Cu2++2e-=Cu,故C错误;
D.Pb(Ac)2溶液中通入H2S时有黑色沉淀生成,发生的离子反应为Pb(Ac)2+H2S=PbS↓+2HAc,故D错误;
故选A.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及复分解反应、电解反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、pH=2的可乐中c(H+)是pH=3的柠檬水中c(H+)的10倍 |
| B、体积相同、pH相同的醋酸和盐酸完全溶解等量的镁粉,后者用时少 |
| C、pH=10的NaOH溶液与pH=12的NaOH的溶液等体积混合后,溶液的pH=11 |
| D、若V1LpH=11的NaOH溶液与V2LpH=3的HA溶液混合后显中性,则V1≤V2 |
要除去KNO3溶液中混有的少量Ba(NO3)2杂质,得到纯净的KNO3溶液,操作正确的是( )
| A、加入适量的Na2CO3溶液,过滤 |
| B、加入足量的K2CO3溶液,过滤 |
| C、先加入过量的K2CO3溶液,过滤,再向滤液中加入适量的稀硝酸 |
| D、先加入过量的K2CO3溶液,过滤,再向滤液中加入适量的稀盐酸 |
在15.2g铁和铜组成的合金中加入过量的硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的NaOH溶液,生成25.4g沉淀.则下列说法不正确的是( )
| A、原合金中含0.1mol Fe、0.15mol Cu |
| B、25.4g沉淀为Cu(OH)2和Fe(OH)3的混合物 |
| C、气体X中含0.3 mol NO、0.1 mol NO2 |
| D、气体X中含0.3 mol NO2、0.1 mol NO |
下述实验方案能达到实验目的是.( )
| 编号 | A | B | C | D |
| 实验 方案 |  | 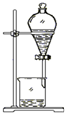 | 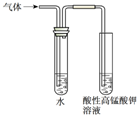 | 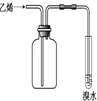 |
| 实验 目的 | 实验室制备乙酸乙酯 | 分离乙酸和水 | 验证溴乙烷在氢氧化钠乙醇溶液中发生消去反应产生的乙烯 | 收集乙烯并验证它与溴水发生加成反应 |
| A、A | B、B | C、C | D、D |
下列有关实验叙述正确的是( )
| A、除去苯中混有的苯酚可加入浓溴水后过滤 |
| B、向酸性KMnO4溶液中滴加维生素C溶液,KMnO4溶液褪色,说明维生素C有还原性 |
| C、向淀粉溶液中滴加稀硫酸后,加热,再加入新制Cu(OH)2加热,没有出现红色沉淀,说明淀粉没有发生水解反应 |
| D、向NaOH溶液中加入溴乙烷,加热,再加入AgNO3溶液,产生沉淀,说明溴乙烷发生了水解反应 |
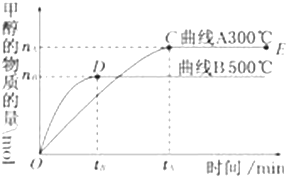 (1)一定条件下,在体积为4L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g).
(1)一定条件下,在体积为4L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g).