题目内容
某同学为了检验家中的一瓶补铁药(成分为FeSO4)是否变质,查阅了有关资料,得知Fe2+能被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,并结合已学的知识设计了如下实验:将药片除去糖衣研细后,溶解过滤,取滤液分别加入两支试管中,在一支试管中滴入酸性高锰酸钾溶液,在另一支试管中滴入KSCN溶液.请你填出该同学实验中出现以下现象时的应得结论:
①若滴入酸性高锰酸钾溶液后褪色,滴入KSCN溶液后不变红,结论是 .
②若滴入酸性高锰酸钾溶液后不褪色,滴入KSCN溶液变红,结论是
③若滴入酸性高锰酸钾溶液后褪色,滴入KSCN溶液变红,结论是 .
①若滴入酸性高锰酸钾溶液后褪色,滴入KSCN溶液后不变红,结论是
②若滴入酸性高锰酸钾溶液后不褪色,滴入KSCN溶液变红,结论是
③若滴入酸性高锰酸钾溶液后褪色,滴入KSCN溶液变红,结论是
考点:二价Fe离子和三价Fe离子的检验
专题:物质检验鉴别题
分析:Fe2+具有还原性,能使高锰酸钾褪色;Fe3+使KSCN溶液变红是三价铁离子的特征反应,可用此判断三价铁离子是否存在.
解答:
解:加KMnO4溶液只要褪色就说明含有Fe2+,而加入KSCN溶液变红则说明含有Fe3+.
(1)根据实验现象分析,高锰酸钾褪色说明有Fe2+;KSCN溶液不变红,说明没有Fe3+;从而确定药品没有被氧化.
故答案为:Fe2+没有被氧化;
(2)根据实验现象分析,高锰酸钾不褪色说明没有Fe2+;KSCN溶液变红,说明有Fe3+;从而确定药品完全被氧化.
故答案为:Fe2+完全被氧化;
(3)根据实验现象分析,高锰酸钾褪色说明有Fe2+;KSCN溶液变红,说明有Fe3+;从而确定药品部分被氧化.
故答案为:Fe2+部分被氧化.
(1)根据实验现象分析,高锰酸钾褪色说明有Fe2+;KSCN溶液不变红,说明没有Fe3+;从而确定药品没有被氧化.
故答案为:Fe2+没有被氧化;
(2)根据实验现象分析,高锰酸钾不褪色说明没有Fe2+;KSCN溶液变红,说明有Fe3+;从而确定药品完全被氧化.
故答案为:Fe2+完全被氧化;
(3)根据实验现象分析,高锰酸钾褪色说明有Fe2+;KSCN溶液变红,说明有Fe3+;从而确定药品部分被氧化.
故答案为:Fe2+部分被氧化.
点评:本题考查了二价铁离子和三价铁离子的检验,难度不大,三价铁离子的检验是高考的热点,常在实验题中考查.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
我们常在公共场所见到下列标志,其中属于回收标志的是( )
A、 |
B、 |
C、 |
D、 |
下列叙述正确的是( )
A、硝基苯的结构简式为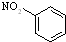 |
| B、只用一种试剂可鉴别苯、苯酚、己烯 |
| C、用质谱法可鉴别1-丙醇和2-丙醇 |
D、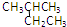 系统命名为2-乙基丙烷 系统命名为2-乙基丙烷 |
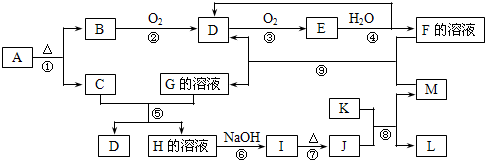
 已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A与B;C、D与E分别位于同一周期.A原子L层上有2对成对电子,B、C、D的核外电子排布相同的简单离子可形成一种C3DB6型离子晶体X,CE、FA为电子数相同的离子晶体.
已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A与B;C、D与E分别位于同一周期.A原子L层上有2对成对电子,B、C、D的核外电子排布相同的简单离子可形成一种C3DB6型离子晶体X,CE、FA为电子数相同的离子晶体.