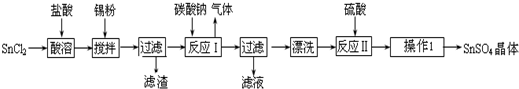
题目内容
2.为分析 空气质量情况,化学研究性学习小组的同学拟测定城市上空空气中SO2的含量,制定了下列研究方案:①相关文献调研:了解空气中主要污染指标,其中SO2对人体有哪些危害;了解SO2的化学性质,为测定SO2的含量寻找理论依据[资料表明,SO2具有较强的还原性,能与酸性KMnO4溶液(紫红色,其还原产物Mn2+在水溶液中接近无色)发生如下反应:5SO2+2MnO4-+2H2O═5SO42-+2Mn2++4H+].
②设计实验方案:利用SO2的还原性进行定量分析.
③选择分析地点:某工业区、某公园、某居民小区、某商业区、某交通枢纽.
④选择分析时间:晴天、风速较小时;晴天、风速较大时;雨前;雨后.
⑤对测定的结果进行初步分析并向相关单位提出建议.
请你参与该研究性学习小组的活动并发表你的见解:
(1)该小组的同学拟用下列装置测定空气中SO2的含量:
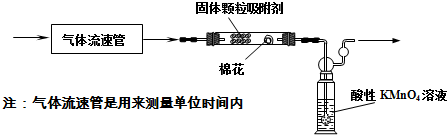
①连接好装置,在装入药品前应进行的实验操作是检查装置的气密性;
②当看到KMnO4溶液刚好褪色现象时,应停止通空气;
实验过程中需测量并记录的数据通人空气至酸性KMnO4溶液刚好褪色所需要的时间(高锰酸钾的物质的量浓度和体积均已知).
(2)如图是该小组同学根据实验测得的不同地区空气中SO2含量:
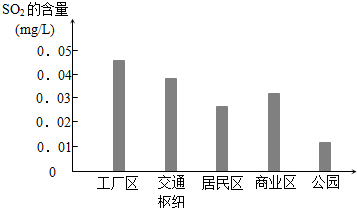
①工厂区SO2含量明显高于其他地区的原因是工厂尾气、汽车尾气中SO2含量较高;
②请你向当地有关部门提出一条减少工厂区SO2排放的建议提高脱硫技术.
分析 设计实验方案:测定二氧化硫的存在,可利用二氧化硫具有漂白性和还原性的角度分析;
(1)①实验前应检查装置的气密性;
②KMnO4具有强氧化性,二氧化硫具有还原性,两者发生反应,KMnO4溶液褪色;
③测出二氧化硫的物质的量以及空气的体积即可求出空气中SO2含量;
(2)①工厂尾气、汽车尾气中SO2含量较高;
②改用更洁净的能源减少SO2的排放.
解答 解:设计实验方案:测定二氧化硫的存在,可利用二氧化硫具有漂白性和还原性的性质,利用SO2使品红溶液褪色作定性分析,只要是利用了二氧化硫的漂白性,可品红溶液反应生成无色物质,
(1)①实验前应检查装置的气密性,以确保装置不漏气,以防止影响结果,故答案为:检查装置的气密性;
②KMnO4具有强氧化性,二氧化硫具有还原性,两者发生反应,所以看到KMnO4溶液刚好褪色时,说明二氧化硫和恰好KMnO4溶液完全反应,应停止通空气,二氧化硫的物质的量可以根据KMnO4的物质的量进行求出,而空气的体积需要知道单位时间内空气的流速和时间来计算,所以需要知道酸性KMnO4溶液刚好褪色所需要的时间,
故答案为:KMnO4溶液刚好褪色,通人空气至酸性KMnO4溶液刚好褪色所需要的时间;
(2)①因工厂尾气中含有大量的SO2、汽车尾气中SO2含量也较高,所以工厂区、交通枢纽SO2含量明显高于其他地区,
故答案为:工厂尾气、汽车尾气中SO2含量较高;
②SO2来源于化石燃料的燃烧,可通过环保能源来减少SO2的排放,或对燃煤进行脱硫处理,
故答案为:提高脱硫技术.
点评 本题综合考查了二氧化硫含量的测定以及二氧化硫的来源与危害,侧重于学生的分析能力的考查,题目涉及化学与生活、环境保护的考查,有利于培养学生的良好的科学素养,提高学习的积极性,难度中等.

练习册系列答案
 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
2.冬天用煤炉取暖时要预防发生一氧化碳中毒事故.一氧化碳的产生主要是因为煤炉中发生了以下反应:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO,试分析下列有关叙述中确的是( )
| A. | C在O2充足时,发生的反应主要是放热反应 | |
| B. | 煤燃烧时吹入的氧气越多越好 | |
| C. | CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO这一反应属于吸热反应 | |
| D. | 煤燃烧时,反应物自身总能量高于生成物总能量,所以放出热量 |
10.下列实验操作中错误的是( )
| A. | 向碘水中加入适量酒精,可以将碘单质萃取出来 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| D. | 蒸发时,当溶液中出现大量晶体时,停止加热余热蒸干 |
17.下列离子组在一定条件下不能大量共存,且所给离子方程式能说明不能共存原因的是( )
| 选项 | 条件 | 离子组 | 共存所发生的离子反应方程式 |
| A | pH=1的溶液 | Fe2+、Al3+、Cl-、MnO4- | 10Cl-+2MnO4-+16H+═2Mn2++5Cl2↑+8H2O |
| B | 能与铝反应生成氢气的溶液 | K+、NO3-、Cl-、NH4+ | NH4++OH-═NH3•H2O |
| C | 常温下c(H+)/c(OH)-=10-10的溶液 | Na+、Cl-、S2-、SO32- | SO32-+2S2-+6H+═3S↓+3H2O |
| D | 含有大量H+的透明溶液 | Na+、Cu2+、AlO2-、SiO32- | 2H++SiO32-═H2SiO3↓ |
| A. | A | B. | B | C. | C | D. | D |
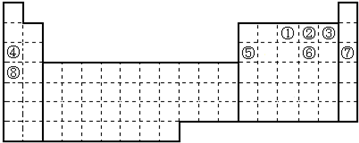
7.Ge 和Sn 的熔点( )
| A. | 大于 | B. | 小于 | C. | 等于 | D. | 不能肯定 |
 .
.