题目内容
14.下列化学用语表述正确的是( )| A. | 甲烷的球棍模型: | B. | 氯化氢的电子式: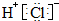 | ||
| C. | Cl2的结构式:Cl=Cl | D. | 硫离子的结构示意图: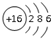 |
分析 A.甲烷分子中,C的原子半径大于H原子;
B.氯化氢为共价化合物,分子中含有1个H-Cl键;
C.氯气的氯原子间为单键;
D.硫离子的核外有18个电子.
解答 解:A.球棍模型表现原子间的连接与空间结构,甲烷分子式为CH4,C原子形成4个C-H,为正四面体结构,碳原子半径大于氢原子半径,球棍模型为 ,故A正确;
,故A正确;
B、HCl分子中含有1个H-Cl键,氯化氢的电子式为 ,故B错误;
,故B错误;
C、氯气是氯原子之间通过共用电子对形成的直线型非极性分子,结构式分别为:Cl-Cl,故C错误;
D、硫离子是硫原子得2个电子后形成的,故核外有18个电子,故结构示意图为 ,故D错误.
,故D错误.
故选A.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及结构式、电子式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生规范答题的能力.

练习册系列答案
相关题目
4.下列离子方程式正确的是( )
| A. | 浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+$\frac{\underline{\;\;△\;\;}}{\;}$Fe3++3NO2↑+3H2O | |
| B. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ | |
| C. | 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2 OH-+NH4++HCO3-═BaCO3↓+NH3•H2O+H2O | |
| D. | 用FeCl3溶液腐蚀印刷电路板:Fe3++Cu═Fe2++Cu2+ |
9.常温下能与浓硫酸发生剧烈反应的金属单质是( )
| A. | Cu | B. | C | C. | Fe | D. | Mg |
19.实验室用NaOH固体和蒸馏水准确配制一定物质的量浓度的NaOH溶液时,以下仪器中不需要用到的是( )
| A. | 托盘天平 | B. | 锥形瓶 | C. | 烧杯 | D. | 容量瓶 |
6.下列说法正确的是( )
| A. | 镁着火后可用二氧化碳灭火器进行灭火 | |
| B. | 焰色反应时,先用稀硫酸洗涤铂丝并在酒精灯火焰上灼烧,然后再进行实验 | |
| C. | 食盐水中混有Mg2+、Ca2+、SO42-,可依次加入过量Ba(OH)2溶液、Na2CO3溶液和适量盐酸,过滤后即可得到精制的食盐水 | |
| D. | 现代化学分析测试中,常借助一些仪器来分析化学物质的组成.如用原子吸收光谱确定物质中含有哪些金属元素 |
2.下列物质属于电解质并能导电的是( )
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤KCl晶体 ⑥液态氯化氢.
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤KCl晶体 ⑥液态氯化氢.
| A. | ① | B. | ①⑥ | C. | ①②⑤ | D. | ①②③⑤ |

 .
.