题目内容
17.将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系.下列判断不正确的是( )| A. | 若反应中转移的电子为n mol,则n一定大于0.15 mol | |
| B. | n(NaCl):n(NaClO):n(NaClO3)可能为7:2:1 | |
| C. | 与NaOH反应的氯气一定为0.15 mol | |
| D. | n(Na+):n(Cl-) 可能为7:3 |
分析 A.利用极限法解答,根据方程式Cl2+2NaOH=NaCl+NaClO+H2O、3Cl2+6NaOH=5NaCl+NaClO3+3H2O可知,氧化产物只有NaClO,转移电子数最少,氧化产物只有NaClO3,转移电子数最多;
B.令n(NaCl)=7mol,n(NaClO)=2mol,n(NaClO3)=1mol,根据转移电子守恒验证;
C.由于反应后体系中没有NaOH,故氢氧化钠反应完,根据钠元素守恒n(NaOH)=n(NaCl)+n(NaClO)+n(NaClO3),再根据氯原子守恒有2n(Cl2)=n(NaCl)+n(NaClO)+n(NaClO3),据此计算;
D.根据方程式Cl2+2NaOH=NaCl+NaClO+H2O、3Cl2+6NaOH=5NaCl+NaClO3+3H2O可知,氧化产物只有NaClO,n(Na+):n(Cl-)最大为2:1,当氧化产物为NaClO3,n(Na+):n(Cl-)最小为6:5,据此判断.
解答 解:A.根据方程式Cl2+2NaOH=NaCl+NaClO+H2O、3Cl2+6NaOH=5NaCl+NaClO3+3H2O可知,氧化产物只有NaClO,转移电子数最少,为0.3mol×$\frac{1}{2}$×1=0.15mol,氧化产物只有NaClO3,转移电子数最多,为0.3mol×$\frac{5}{6}$×1=0.25mol,实际上n介于二者之间,所以n一定大于0.15 mol,故A正确;
B.令n(NaCl)=7mol,n(NaClO)=2mol,n(NaClO3)=1mol,得到电子的物质的量=n(NaCl)=7mol,失电子的物质的量=n(NaClO)+5n(NaClO3)=2mol+5mol=7mol,得失电子相等,符合转移电子守恒规律,故B正确;
C.由于反应后体系中没有NaOH,故氢氧化钠反应完,根据钠元素守恒n(NaOH)=n(NaCl)+n(NaClO)+n(NaClO3)=0.03L×10mol/L=0.3mol,根据氯原子守恒有2n(Cl2)=n(NaCl)+n(NaClO)+n(NaClO3)=0.3mol,故参加反应的氯气n(Cl2)=0.15mol,故C正确;
D.根据方程式Cl2+2NaOH=NaCl+NaClO+H2O、3Cl2+6NaOH=5NaCl+NaClO3+3H2O可知,氧化产物只有NaClO,n(Na+):n(Cl-)最大为2:1,当氧化产物为NaClO3,n(Na+):n(Cl-)最小为6:5,故6:5<n(Na+):n(Cl-)<2:1,7:3>2:1,故D错误;
故选D.
点评 本题考查化学方程式有关计算,为高频考点,明确各个物理量之间的关系式、转移电子守恒是解本题关键,侧重考查学生分析计算能力,注意极限法的正确运用,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | CO2的电子式为: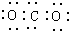 | B. | Cl2的结构式: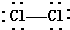 | ||
| C. | 用电子式表示NaCl的形成过程: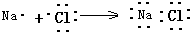 | D. | F-的结构示意图: |
| A. | +45 kJ•mol-1 | B. | +32.7 kJ•mol-1 | C. | -45 kJ•mol-1 | D. | 无法计算 |
| A. | 质子数一定相同,质量数和中子数一定不同 | |
| B. | 化学性质几乎完全相同 | |
| C. | 一定都由质子、中子、电子构成 | |
| D. | 核电荷数,核外电子数一定相同 |
| A. | a=b=c | B. | a>b>c | C. | b>c>a | D. | c>b>a |
| A. | 晶体硅可用于制造光导纤维 | B. | 氯氧化钠用来治疗胃酸过多 | ||
| C. | 铝制容器可以用来贮运稀硝酸 | D. | 乙烯用作水果的催熟剂 |
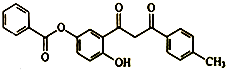
| A. | 分子中含醚键,不含手性碳原子 | |
| B. | 在空气中易被氧化变质 | |
| C. | 能发生取代、加成、消去反应 | |
| D. | 1mol该物质最多能与3mol NaOH溶液发生反应 |
| A. |  | B. |  | C. |  | D. |  |