题目内容
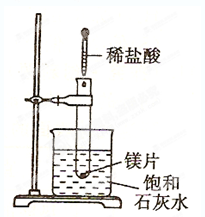
如下图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5 mL盐酸于试管中.试完成下列问题:

(1)实验中观察到的现象是________.
(2)产生上述现象的原因是________.
(3)有关反应的离子方程式为________.
(4)由实验推知,MgCl2溶液和H2的总能量________(填“大于” “小于”或“等于”)镁片和盐酸的总能量.
答案:
解析:
解析:
|
答案:(1)①镁片上有大量气泡产生;②镁片逐渐溶解;③烧杯中析出晶体 (2)镁与盐酸反应生成氢气;该反应为放热反应;Ca(OH)2在水中的溶解度随温度升高而减小,故析出Ca(OH)2晶体 (3)Mg+2H+ (4)小于 思路解析:(1)滴入盐酸后发生反应:Mg+2HCl |

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目