题目内容
(1)若电解足量的氯化铜溶液,写出电解时发生反应的化学方程式 ,如果电解一段时间后,电路中转移2mol的电子,阳极在标准状况下放出氯气 L.
(2)若电解足量的氯化钠溶液,写出电解时发生反应的化学方程式 ,如果电解一段时间后,电路中转移1mol的电子,则阴极析出氢气 L.
(2)若电解足量的氯化钠溶液,写出电解时发生反应的化学方程式
考点:电解原理
专题:电化学专题
分析:(1)电解足量CuCl2溶液时,阳极上氯离子放电、阴极上铜离子放电,相当于电解氯化铜,根据转移电子和氯气之间的关系式计算;
(2)电解足量NaCl溶液时,阳极上氯离子放电、阴极上氢离子放电,根据转移电子和氢气之间的关系式计算.
(2)电解足量NaCl溶液时,阳极上氯离子放电、阴极上氢离子放电,根据转移电子和氢气之间的关系式计算.
解答:
解:(1)电解足量CuCl2溶液时,阳极上氯离子放电、阴极上铜离子放电,相当于电解氯化铜,所以其电池反应式为CuCl2
Cu+Cl2↑,阳极反应式为2Cl--2e-=Cl2↑,设生成氯气体积为x,
2Cl--2e-=Cl2↑
2mol 22.4L
2mol x
2mol:22.4L=2mol:x
x=
=22.4L,
故答案为:CuCl2
Cu+Cl2↑;22.4;
(2)电解足量NaCl溶液时,阳极上氯离子放电、阴极上氢离子放电,电池反应式为2NaCl+2H2O
H2↑+Cl2↑+NaOH,
设生成气体体积为y,
2NaCl+2H2O
H2↑+Cl2↑+NaOH 转移电子
22.4L 2mol
y 1mol
22.4L:2mol=y:1mol
y=
=11.2L,
故答案为:2NaCl+2H2O
H2↑+Cl2↑+NaOH;11.2.
| ||
2Cl--2e-=Cl2↑
2mol 22.4L
2mol x
2mol:22.4L=2mol:x
x=
| 22.4L×2mol |
| 2mol |
故答案为:CuCl2
| ||
(2)电解足量NaCl溶液时,阳极上氯离子放电、阴极上氢离子放电,电池反应式为2NaCl+2H2O
| ||
设生成气体体积为y,
2NaCl+2H2O
| ||
22.4L 2mol
y 1mol
22.4L:2mol=y:1mol
y=
| 22.4L×1mol |
| 2mol |
故答案为:2NaCl+2H2O
| ||
点评:本题以电解原理为载体考查物质的量的计算,明确离子放电顺序及方程式中各个物理量之间的关系式即可解答,注意基础知识的积累,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
地球大气臭氧层集中在离地面20~30km以上的平流层,它消耗太阳向地球辐射的紫外线能量的99%.近年来,臭氧不断减少,在两极出现了臭氧空洞,人类皮肤癌、白内障等疾病患者明显增加,海洋生物减少.这是由于过量紫外线照射( )
| A、引起空气发生化学变化 |
| B、产生杀菌消毒作用 |
| C、诱发动植物的基因突变 |
| D、造成病毒感染 |
铁粉和铜粉的均匀混合物,平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成NO的体积和剩余金属的质量如下表(设硝酸的还原产物只有NO):
下列计算结果错误的是( )
| 编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属/g | 18.0 | 9.6 | 0 | 0 |
| NO体积/mL | 2240 | 4480 | 6720 | V |
| A、实验①中硝酸只和铁粉反应 |
| B、原混合物总质量为105.6g |
| C、硝酸浓度为4mol?L-1 |
| D、V=6720 |
向27.2gCu、CuO、Cu2O的混合物中加入某浓度的稀硝酸0.5L,生成NO和Cu(NO3)2.在所得溶液中加入1.0mol/L的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g,下列说法不正确的是( )
| A、原混合物中Cu和O的物质的量之比为2:1 |
| B、硝酸的物质的量浓度为2.6mol/L |
| C、产生的NO在标准状况下的体积为4.48L |
| D、Cu、CuO、Cu2O与硝酸反应后剩余HNO3为0.2mol |
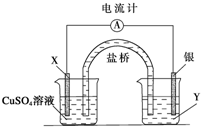 根据下列氧化还原反应2FeCl3+Cu═2FeCl2+CuCl2设计一个原电池:
根据下列氧化还原反应2FeCl3+Cu═2FeCl2+CuCl2设计一个原电池: