题目内容
2.依据氧化还原反应:MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O,欲采用滴定的方法测定FeSO4的质量分数,实验步骤如下:①称量绿矾样品15.2g,配成100mL待测溶液②取10.0ml待测液置于锥形瓶中,并加入一定量的硫酸③将0.1mol•L-1的KMnO4溶液装入滴定管中,调节液面至8.00mL处④滴定待测液至滴定终点时,滴定管的液面读数18.00mL
(1)如何知道滴定到达终点?溶液由浅绿色变为紫红色,且半分钟后不变.
(2)下列操作会导致测定结果偏低的是C
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(3)下列每种量器的数量不限,在上述实验中,必须使用的有ABDE
A.托盘天平 B.量筒 C.碱式滴定管 D.酸式滴定管 E容量瓶
(4)FeSO4的质量分数为50%.
分析 (1)高锰酸钾本身呈紫色,无需指示剂,滴定终点时,颜色变成紫红色,并且半分钟内不褪色即可;
(2)根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$判断不当操作对相关物理量的影响;
(3)根据配制一定物质的量浓度的溶液需要的仪器以及滴定所需要的仪器来解答;
(4)根据5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O计算.
解答 解:(1)高锰酸钾本身呈紫色,无需指示剂,滴定终点时,颜色变成紫红色,并且半分钟内不褪色;
故答案为:溶液由浅绿色变为紫红色,且半分钟后不变;
(2)A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定,标准液浓度减小,造成v(标准)增大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$判断,可知c(待测)偏大,故A错误;
B.锥形瓶用蒸馏水洗涤后未用待测液润洗,所需v(标准)不变,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$判断,可知c(待测)不变,故B错误;
C.读读取标准液读数时,滴定前平视,滴定到终点后俯视,造成v(标准)偏小,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$判断,可知c(待测)偏小,故C正确;
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失,造成v(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$判断,可知c(待测)偏大,故D错误;
故选:C;
(3)配制100mL待测溶液需要的仪器有:托盘天平、药匙、量筒、烧杯、玻璃棒、100ml容量瓶、胶头滴管;滴定所需要的仪器有:酸式滴定管;锥形瓶;铁架台等,
故答案为:ABDE;
(4)由题意可知10.0ml待测液与10.0ml0.1mol•L-1的KMnO4完全反应,
5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O,
5 1
0.01L×C 0.1mol•L-1×0.01L
则C=0.5mol•L-1,则10.0ml待测液中FeSO4的物质的量为0.5mol•L-1×0.01L=0.005mol,FeSO4的质量为0.005mol×152g/mol=0.76g,100mL待测溶液中FeSO4的质量为7.6g,所以样品中FeSO4的质量分数为$\frac{7.6g}{15.2g}$×100%=50%;
故答案为:50%.
点评 本题主要考查氧化还原反应滴定、化学计算等,难度中等,清楚实验原理是解题的关键,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力.

 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度的位置;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度或“0“刻度以下的某一位置.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至溶液刚好变色,测得盐酸的体积为V1mL.
④重复以上过程两次,测得所耗盐酸的体积分别为V2mL、V3mL.试回答下列问题:
(1)锥形瓶中的溶液从红色变为无色时,停止滴定.
(2)滴定时边滴边摇动锥形瓶,眼睛应观察B
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是待测溶液润洗锥形瓶,由此造成的测定结果偏高(偏高、偏低或无影响)
(4)步骤②缺少的操作是未用标准液润洗酸式滴定管由此造成的测定结果偏高(偏高、偏低或无影响)
(5)如图,是某次滴定时的滴定管中的液面,其读数为22.60mL
(6)根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.00 | 19.90 |
| 第二次 | 25.00 | 0.00 | 20.00 |
| 第三次 | 25.00 | 4.00 | 24.10 |
| A. | 铍(Be)的原子失电子能力比镁弱 | |
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 | |
| C. | 氢氧化锶[Sr(OH)2]比氢氧化钙的碱性强 | |
| D. | 硒(Se)化氢比硫化氢稳定 |
| A. | 煤燃烧是热能转化为化学能的过程 | |
| B. | 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程 | |
| C. | 植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程 | |
| D. | 化石燃料属于一次能源,电能属于二次能源 |
 .
.
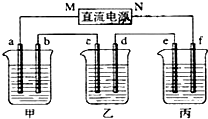
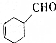 $→_{催化剂}^{H_{2}(足量)}$A$\stackrel{HBr}{→}$B$→_{干醚}^{Mg}$
$→_{催化剂}^{H_{2}(足量)}$A$\stackrel{HBr}{→}$B$→_{干醚}^{Mg}$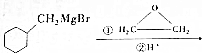 C$→_{Cu,△}^{O_{2}}$
C$→_{Cu,△}^{O_{2}}$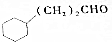 $→_{H+}^{KMnO_{4}}$D$→_{浓H_{2}SO_{4},△}^{E}$
$→_{H+}^{KMnO_{4}}$D$→_{浓H_{2}SO_{4},△}^{E}$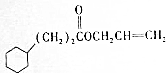
 RCH2CH2OH+
RCH2CH2OH+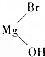
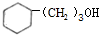 .
. 的化学方程式2
的化学方程式2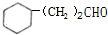 +2H2O,反应类型为氧化反应.
+2H2O,反应类型为氧化反应. ,反应类型为酯化反应.
,反应类型为酯化反应. ,名称为丙酮.
,名称为丙酮.