题目内容
汽车尾气里含有NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:
N2(g)+O2(g)?2NO(g)△H>0
已知该反应在2404℃时,平衡常数K=64×10-4.请回答:
(1)该反应的平衡常数表达式为
(2)该温度下,向2L密闭容器中充入N2和O2各1mol,平衡时,N2的转化率是 %(保留整数).
(3)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应 填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”)
(4)将N2、O2的混合气体充入恒温恒容密闭容器中,如图甲所示变化趋势正确的是 (填字母序号).

(5)该反应的反应过程中能量变化如图乙所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是 .
A.该反应为放热反应
B.催化剂能降低该反应的活化能
C.催化剂能改变该反应的焓变
D.逆反应的活化能小于正反应的活化能
(6)三效催化转化器可减少汽车尾气中的主要污染物(CO、NOx等),反应如下:2NO(g)+2CO(g)═N2(g)+2CO2(g)
已知:
N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol
2C(s)+O2(g)=2CO(g)△H=-221.kJ/mol
C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
则该反应的△H= .
N2(g)+O2(g)?2NO(g)△H>0
已知该反应在2404℃时,平衡常数K=64×10-4.请回答:
(1)该反应的平衡常数表达式为
(2)该温度下,向2L密闭容器中充入N2和O2各1mol,平衡时,N2的转化率是
(3)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应
(4)将N2、O2的混合气体充入恒温恒容密闭容器中,如图甲所示变化趋势正确的是

(5)该反应的反应过程中能量变化如图乙所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是
A.该反应为放热反应
B.催化剂能降低该反应的活化能
C.催化剂能改变该反应的焓变
D.逆反应的活化能小于正反应的活化能
(6)三效催化转化器可减少汽车尾气中的主要污染物(CO、NOx等),反应如下:2NO(g)+2CO(g)═N2(g)+2CO2(g)
已知:
N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol
2C(s)+O2(g)=2CO(g)△H=-221.kJ/mol
C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
则该反应的△H=
考点:化学平衡的计算,反应热和焓变,用盖斯定律进行有关反应热的计算
专题:化学反应中的能量变化,化学平衡专题
分析:(1)依据化学方程式和平衡常数概念列式;
(2)依据平衡三段式列式计算平衡浓度得到平衡常数;
(3)依据浓度商计算和平衡常数比较判断反应进行的方向;
(4)根据温度、催化剂对反应速率和平衡移动的影响判断;
(5)A、依据图象中反应物和生成物能量的大小比较判断;
B、催化剂改变速率不改变平衡;
C、催化剂改变化学反应速率是降低了反应的活化能;
D、图象中分析判断;
(6)依据热化学方程式和 盖斯定律计算得到所需让化学方程式;
(2)依据平衡三段式列式计算平衡浓度得到平衡常数;
(3)依据浓度商计算和平衡常数比较判断反应进行的方向;
(4)根据温度、催化剂对反应速率和平衡移动的影响判断;
(5)A、依据图象中反应物和生成物能量的大小比较判断;
B、催化剂改变速率不改变平衡;
C、催化剂改变化学反应速率是降低了反应的活化能;
D、图象中分析判断;
(6)依据热化学方程式和 盖斯定律计算得到所需让化学方程式;
解答:
解:(1)N2(g)+O2(g)?2NO(g)△H>0
反应的平衡常数K=
;
故答案为:
;
(2)该温度下,向2L密闭容器中充入N2和O2各1mol,平衡时,N2的转化率设为x
N2(g)+O2(g)?2NO(g)
起始量(mol/L) 0.5 0.5 0
转化量(mol/L) 0.5x 0.5x x
平衡量(mol/L) 0.5-0.5x 0.5-0.5x x
K=
=64×10-4,计算x=0.04=4%;
故答案为:4%;
(3)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,Q=
=9×10-4<K=64×10-4,此时反应正向进行;
故答案为:向正反应方向进行;
(4)A、该反应的正反应为吸热反应,则升高温度平衡向正反应进行,平衡常数增大,故A正确;
B、加入催化剂,反应速率增大,但平衡不发生移动,故B错误;
C、升高温度,反应速率增大,平衡向正反应方向移动,氮气的转化率增大,故C正确.
故答案为:AC;
(5)A、图象中反应物能量低于生成物能量,故反应是吸热反应,故A错误;
B、催化剂改变化学反应速率是降低了反应的活化能,故B正确;
C、催化剂不能改变该反应的焓变,只能改变反应速率,故C错误;
D、图象分析逆反应的活化能E2小于正反应的活化能E1,故D正确;
故答案为:BD;
(6)①N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol
②2C(s)+O2(g)=2CO(g)△H=-221.kJ/mol
③C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
依据盖斯定律③×2-②-①得到:2NO(g)+2CO(g)═N2(g)+2CO2(g)△H=-746.5kJ?mol-1;
故答案为:-746.5kJ?mol-1;
反应的平衡常数K=
| c2(NO) |
| c(N2)c(O2) |
故答案为:
| c2(NO) |
| c(N2)c(O2) |
(2)该温度下,向2L密闭容器中充入N2和O2各1mol,平衡时,N2的转化率设为x
N2(g)+O2(g)?2NO(g)
起始量(mol/L) 0.5 0.5 0
转化量(mol/L) 0.5x 0.5x x
平衡量(mol/L) 0.5-0.5x 0.5-0.5x x
K=
| x2 |
| (0.5-0.5x)2 |
故答案为:4%;
(3)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,Q=
| (3.0×10-3)2 |
| 2.5×10-1×4.0×10-2 |
故答案为:向正反应方向进行;
(4)A、该反应的正反应为吸热反应,则升高温度平衡向正反应进行,平衡常数增大,故A正确;
B、加入催化剂,反应速率增大,但平衡不发生移动,故B错误;
C、升高温度,反应速率增大,平衡向正反应方向移动,氮气的转化率增大,故C正确.
故答案为:AC;
(5)A、图象中反应物能量低于生成物能量,故反应是吸热反应,故A错误;
B、催化剂改变化学反应速率是降低了反应的活化能,故B正确;
C、催化剂不能改变该反应的焓变,只能改变反应速率,故C错误;
D、图象分析逆反应的活化能E2小于正反应的活化能E1,故D正确;
故答案为:BD;
(6)①N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol
②2C(s)+O2(g)=2CO(g)△H=-221.kJ/mol
③C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
依据盖斯定律③×2-②-①得到:2NO(g)+2CO(g)═N2(g)+2CO2(g)△H=-746.5kJ?mol-1;
故答案为:-746.5kJ?mol-1;
点评:本题考查了化学平衡、反应速率、平衡常数影响因素和计算应用,化学反应的能量变化分析,催化剂的作用实质,图象识别和理解含义是解题关键,题目难度中等.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
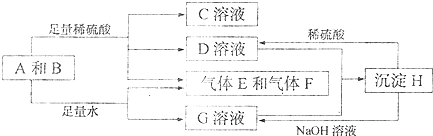
 二甲醚(CH3OCH3)被称为21世界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
二甲醚(CH3OCH3)被称为21世界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应: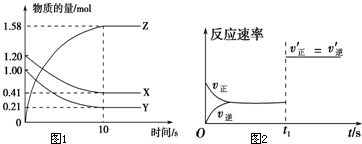 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图1所示:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图1所示: