题目内容
20.取一定质量的Fe2O3,在高温下用CO还原一段时间后得到1.84g固体物质X,将X全部溶于稀硫酸中,经测定消耗H2SO40.0300mol,放出H20.448L(已经折算成标准状况下的体积),所得溶液中滴加KSCN溶液,无血红色出现(已知Fe3+遇SCN-会使溶液呈血红色).试计算:(1)1.84gX中含Fe元素的质量为1.12g.
(2)X物质中除含Fe外,还可能含有的物质是Fe2O3.
分析 (1)据Fe+H2SO4=FeSO4+H2↑,中氢气的量算出生成固体铁的质量;
(2)消耗硫酸的物质的量为n(H2SO4)=0.0300mol,向反应所得溶液加KSCN溶液无血红色出现,说明溶液为FeSO4溶液,根据硫元素守恒可知n(FeSO4)=n(H2SO4)=0.0300mol,根据铁元素守恒可知n(Fe)=2n(Fe2O3)=n(FeSO4),据此结合m=nM计算得到的Fe2O3的质量,并联系(1)分析固体可能含有的物质.
解答 解:(1)Fe+H2SO4=FeSO4+H2↑
56 22.4
1.12 0.448
则:m(Fe)=1.12g,故答案为:1.12;
(2)消耗硫酸的物质的量为n(H2SO4)=0.0300mol,向反应所得溶液加KSCN溶液无血红色出现,说明溶液为FeSO4溶液,根据硫元素守恒可知n(FeSO4)=n(H2SO4)=0.0300mol,根据铁元素守恒可知n(Fe)=2n(Fe2O3)=n(FeSO4)=)=0.0300mol,故n(Fe2O3)=$\frac{0.03mol}{2}$=0.015mol,
m(Fe2O3)=0.015mol×160g/mol=2.4g,m(Fe)=1.12g,固体物质X质量1.84g,介于1.12g~2.4g,故X物质中除含Fe外,还可能含有的物质是Fe2O3,
故答案为:Fe2O3.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应实质为解答关键,注意掌握守恒思想在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
10.常温下.弱碱MOH的电离常数K=1.0×10-3,0.1mol•L-1 MOH溶液的pH约为( )
| A. | 8 | B. | 9 | C. | 11 | D. | 12 |
11.某含铬Cr2O72- 废水用硫酸亚铁铵[FeSO4•(NH4)2 SO4•6H2O]处理,反应中铁元素和铬元素完全转化为沉淀.该沉淀干燥后得到n molFeO•FeyCrxO3.不考虑处理过程中的实际损耗,下列叙述正确的是( )
| A. | 消耗硫酸亚铁铵的物质的量为n(2-x)mol | |
| B. | 处理废水中Cr2O72- 的物质的量为nxmol | |
| C. | 反应中发生转移的电子数为3n mol | |
| D. | 在FeO•FeyCrxO3中3x=y |
9.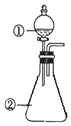 用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
 用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
| B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
| C | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
| D | 亚硫酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
| A. | A | B. | B | C. | C | D. | D |
10.铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.请回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g)?Fe(s)+CO2(g) K1△H1=a KJ•mol-1
3Fe2O3(s)+CO(g)?2Fe3O4(s)+CO2(g) K2△H2=b KJ•mol-1
Fe3O4(s)+CO(g)?3FeO(s)+CO2(g) K3△H3=c KJ•mol-1
①Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=$\frac{6a+b+2c}{3}$KJ•mol-1(用含a、b、c的代数式表示).
②上述反应对应的平衡常数K1、K2、K3随温度变化的曲线如图1所示.则a>b,(填“>”、“<”或“=”),理由是由图可知,随着温度的升高,K1增大、K2减小,则△H1>0、△H2<0,所以a>b.
(2)铁的氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应,如图2,下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是b.

(3)铁等金属可用作CO与H2反应的催化剂:CO(g)+3H2(g)?CH4(g)+H2O(g)△H<0.在T℃,将l mol CO和3mol H2加入2L的密闭容器中.实验测得n(CO)随时间的变化如表:
①下列能判断该反应达到平衡的标志是ad(填序号).
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(CO)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
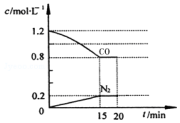
②在0~20min内v (H2)=0.04mol•L-1•min-1;在T℃时该反应的平衡常数K=1200.
③图3表示该反应中CO的转化率与温度、压强的关系.图中压强P1、P2、P3由高到低的顺序是P1>P2>P3.
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g)?Fe(s)+CO2(g) K1△H1=a KJ•mol-1
3Fe2O3(s)+CO(g)?2Fe3O4(s)+CO2(g) K2△H2=b KJ•mol-1
Fe3O4(s)+CO(g)?3FeO(s)+CO2(g) K3△H3=c KJ•mol-1
①Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=$\frac{6a+b+2c}{3}$KJ•mol-1(用含a、b、c的代数式表示).
②上述反应对应的平衡常数K1、K2、K3随温度变化的曲线如图1所示.则a>b,(填“>”、“<”或“=”),理由是由图可知,随着温度的升高,K1增大、K2减小,则△H1>0、△H2<0,所以a>b.
(2)铁的氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应,如图2,下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是b.

(3)铁等金属可用作CO与H2反应的催化剂:CO(g)+3H2(g)?CH4(g)+H2O(g)△H<0.在T℃,将l mol CO和3mol H2加入2L的密闭容器中.实验测得n(CO)随时间的变化如表:
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| n(CO)/mol | 1.0 | 0.70 | 0.45 | 0.25 | 0.10 | 0.10 |
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(CO)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②在0~20min内v (H2)=0.04mol•L-1•min-1;在T℃时该反应的平衡常数K=1200.
③图3表示该反应中CO的转化率与温度、压强的关系.图中压强P1、P2、P3由高到低的顺序是P1>P2>P3.

 回答下列问题:
回答下列问题: 北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).