题目内容
7.最近,我国利用生产磷铵排放的废渣磷石膏制取硫酸并联产水泥的技术研究获得成功.已知磷灰石的主要成分是Ca3(PO4)2.具体生产流程如图1:
回答下列问题:
(1)装置a用磷酸吸收NH3.若该过程在实验室中进行,请画出装置a的示意图.
(2)热交换器是实现冷热交换的装置.化学实验中也经常利用热交换来实现某种实验目的,如气、液热交换时通常使用的仪器是冷凝管;
(3)依题意猜测固体A中一定含有的物质的化学式是CaSO4(结晶水部分不写).
(4)利用生产磷铵排放的废渣磷石膏制取硫酸,其中SO2生产硫酸的工艺流程图如图2所示:
①在A处二氧化硫被氧化成三氧化硫,设备A的名称是接触室,设备A中发生反应的化学方程式是2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3,为提高三氧化硫的产率,该处应采用等温过程(填“等温过程”或“绝热过程”)为宜.
②在D处进行二次催化处理的原因是该反应为可逆反应,二次催化使尚未反应的SO2尽量催化氧化成SO3,可以降低成本提高原料利用率和保护环境;
③B处气体混合物主要是氮气和三氧化硫.此时气体经过C后不立即进入D是因为:通过吸收塔C后,混合气体中SO3含量较多,不利于SO2的催化氧化反应进行;
④20%的发烟硫酸(SO3的质量分数为20%)1吨需加水0.066吨(保留2位有效数字)才能配制成98%的成品硫酸.
(5)制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾.能用于测定硫酸尾气中SO2含量的是BC(选填字母)
A.NaOH溶液、酚酞试液
B.KMnO4溶液、稀H2SO4
C.碘水、淀粉溶液
D.氨水、酚酞试液.
分析 磷灰石粉碎富集后,在萃取槽中用硫酸酸化得到硫酸钙与磷酸,过滤分离得到固体A为石膏与磷酸.装置a中磷酸与氨气发生反应,可以生成(NH4)3PO4、(NH4)2HPO4、NH4H2PO4,操作b是由溶液中析出晶体,应萃取蒸发浓缩、冷却结晶等操作,铵盐受热容易分解,在结晶时应采用低温蒸发结晶.在经过过滤分离得到磷酸铵,分离得到滤液进行循环利用,石膏经过一系列工艺得到水泥,得到二氧化硫等气体,气体处理后在热交换器中发生催化氧化得到三氧化硫,三氧化硫转化为硫酸,再循环利用,
(1)磷酸和氨气极易反应,会产生倒吸的危险;
(2)冷凝管能实现气、液热交换;
(3)由信息可知生产磷铵排放的废渣磷石膏制取硫酸,磷灰石的主要成分是Ca3(PO4)2,在萃取槽中与硫酸发生反应,有磷酸生成,结合流程中硫酸制备,故固体A应为CaSO4;
(4)①二氧化硫在接触室中被氧化成三氧化硫,化学方程式为2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3,该反应为放热反应,升高温度,平衡逆向移动,不利于提高三氧化硫的产率;
②2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3为可逆反应,从提高产率和环境保护角度分析;
③通过吸收塔C后,混合气体中SO3含量较多,分析对2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3平衡移动的影响;
④1吨20%的发烟硫酸中含SO3的质量为0.2t,加水后可生成H2SO40.245t,即硫酸的总质量为1.045t,换算为98%的浓硫酸质量为1.045t÷98%=1.066t.
(5)SO2、微量的SO3和酸雾都能与碱反应,不能利用碱测定,SO2具有还原性,可以利用强氧化剂测定.
解答 解:(1)磷酸和氨气极易反应,为防止反应过于迅速会产生倒吸的危险,要采用防倒吸装置,装置a图为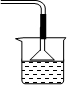 ,
,
故答案为: ;
;
(2)能实现气、液热交换的装置是冷凝管,下口进水伤口处谁,气体和水流方向相反,故答案为:冷凝管;
(3)由信息可知生产磷铵排放的废渣磷石膏制取硫酸,磷灰石的主要成分是Ca3(PO4)2,在萃取槽中与硫酸发生反应,有磷酸生成,结合流程中硫酸制备,故固体A应为CaSO4.
故答案为:CaSO4;
(4)①二氧化硫在接触室中被氧化成三氧化硫,化学方程式为2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3,该反应为放热反应,升高温度,平衡逆向移动,不利于提高三氧化硫的产率,因此应选择等温过程,
故答案为:接触室;2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3;等温过程;
②2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3为可逆反应,二次催化使尚未反应的SO2尽量催化氧化成SO3,可以降低成本提高原料利用率和保护环境,
故答案为:该反应为可逆反应,二次催化使尚未反应的SO2尽量催化氧化成SO3,可以降低成本提高原料利用率和保护环境;
③通过吸收塔C后,混合气体中SO3含量较多,由2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3可知,不利于平衡正向移动,
故答案为:通过吸收塔C后,混合气体中SO3含量较多,不利于SO2的催化氧化反应进行;
④1吨20%的发烟硫酸中含SO3的质量为0.2t,硫酸为0.8t,加水后可生成H2SO40.245t,即硫酸的总质量为1.045t,换算为98%的浓硫酸质量为$\frac{1.045t}{98%}$=1.066t,故加入的水的质量为0.066t,
故答案为:0.066;
(5)A、NaOH溶液与SO2、微量的SO3和酸雾反应,测量的SO2含量偏高,故A错误;
B、硫酸尾气中只有SO2能被酸性KMnO4溶液氧化,溶液颜色由紫红色变为无色,根据KMnO4溶液的体积结合方程式计算SO2的含量,故B正确;
C、硫酸尾气中只有SO2能被碘水氧化SO2,溶液颜色由蓝色变为无色,根据碘水溶液的体积结合方程式计算SO2的含量,故C正确;
D、氨水NaOH溶液与SO2、微量的SO3和酸雾反应,测量的SO2含量偏高,故D错误.
故答案为:BC.
点评 本题考查了化学工业生产流程的分析、实验操作以及产物的判断和计算,综合性强,为高考高频考点,掌握工业制取硫酸、磷铵的原理和流程是解题的关键,难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 一定温度、压强下,气体体积由其物质的量的多少决定 | |
| B. | 两种物质的物质的量相同,则它们在标准状况下的体积相同 | |
| C. | 同温同压下,气体的密度与气体的相对分子质量成正比 | |
| D. | 同温同体积时,气体物质的物质的量越大,则压强越大 |
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/(g.cm-3) | 水溶性 | |
| 苯甲酸 | 122 | 122.4 | 249 | 1.2659 | 微溶 |
| 甲醇 | 32 | -97 | 64.6 | 0.792 | 互溶 |
| 苯甲酸甲酯 | 136 | -12.3 | 196.6 | 1.0888 | 不溶 |
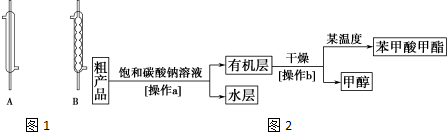
(1)实验中,应选择(如图1)B(填序号)作为冷凝回流装置,该仪器的名称为球形冷凝管.
(2)使用过量甲醇的原因是甲醇沸点低,损失大;甲醇过量可以提高苯甲酸的利用率.
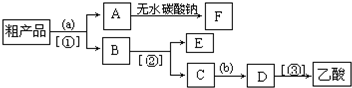
Ⅱ.粗产品的精制 苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图2进行精制.
(3)饱和碳酸钠溶液的作用是除去苯甲酸甲酯中的杂质苯甲酸,溶解甲醇,降低苯甲酸甲酯溶解度,操作a的名称为分液.
(4)由于有机层和水层的密度比较接近,兴趣小组的同学无法直接判断有机层在上层还是下层,请你设计简单易行的方案,简述实验方法,可能的现象及结论从分液漏斗下口放出少量液体,置于试管中,加入适量水,振荡、静置,若液体分层,则有机层在下层,若液体不分层,则有机层在上层.
(5)该实验中制得苯甲酸甲酯8.30g,则苯甲酸甲酯的产率为61.0%.
已知:
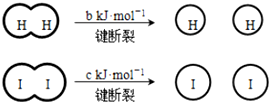 (a、b、c均大于零) 下列说法不正确的是( )
(a、b、c均大于零) 下列说法不正确的是( )| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 断开 1 mol H-H 键和1 mol I-I键所需能量大于断开 2 mol H-I键所需能量 | |
| C. | 断开 2 mol H-I键所需能量约为(c+b+a) kJ | |
| D. | 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于 2a kJ |
| A. | 提高硫酸亚铁的溶解度 | B. | 防止硫酸亚铁分解 | ||
| C. | 抑制硫酸亚铁水解 | D. | 稀硫酸防止硫酸亚铁被氧化 |
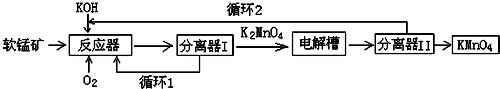
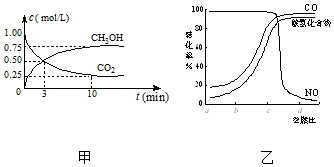 CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径.
CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径.