题目内容
(13分)过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。回答下列有关双氧水的一些问题:
(1)下述反应中,H2O2仅体现氧化性的反应是(填代号)_________。
A.Na2O2+2HCl == 2NaCl+H2O2
B.Ag2O+H2O2== 2Ag+O2↑+H2O
C.2H2O2 == 2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH == 2K2CrO4+3K2SO4+8H2O
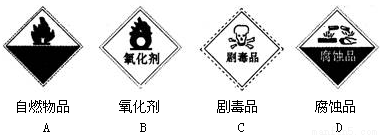
(2)保存过氧化氢的试剂瓶上最适合贴上的一个标签是_________(填字母代号)。
(3)某强酸性反应体系中,反应物和生成物共六种物质或离子:O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2↑。
①写出该反应的离子方程式并配平___________________________________________。
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子数目为_________。
(4)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称,如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+ H2O2+ H2O==A+NH3↑,试指出生成物A的化学式为__________________,并阐明H2O2被称为“绿色氧化剂”的理由是_____________________________________________。
(1)D (2) B(3) ① 6H+ + 2MnO4- + 5H2O2 = 2Mn2+ + 5O2 ↑+ 8H2O
② 3.612×1023(或0.6NA)(4)KHCO3; H2O2作氧化剂时,其还原产物为H2O,.不会产生污染
【解析】
试题分析::(1)A体现双氧水有酸性,它是二元弱酸;B.中双氧水中氧元素化合价升高,说明双氧水作还原剂,体现了还原性;C中双氧水中氧元素化合价升高,体现还原性;D中双氧水中氧元素化合价降低,说明双氧水作氧化剂,体现了氧化性;(2)双氧水常用作氧化剂,具有氧化性,所以用标签B;(3)①H2O2只发生了H2O2→O2的变化体现了双氧水的还原性,做还原剂,所以高锰酸根做氧化剂,还原产物是锰离子,根据氧化还原反应电子守恒配平,6H+ + 2MnO4- + 5H2O2 = 2Mn2+ + 5O2 ↑+ 8H2O ;②双氧水中-1价的氧变为氧气中的0价,当生成6.72L(标准状况)即0.3mol氧气时,则失电子数目为:0.3mol×2×(1-0)=0.6mol,即0.6NA;(4)反应KCN+H2O2+H2O=A+NH3↑遵循原子守恒,所以A为KHCO3,双氧水做氧化剂的还原产物为水,无污染。
考点:考查氧化还原反应及有关反应。

 之和为1 mol?
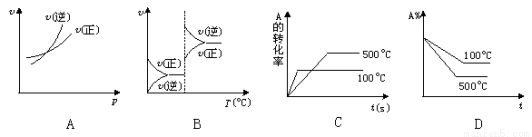
之和为1 mol? 2C(g) ΔH﹥0,下列图象中正确的是
2C(g) ΔH﹥0,下列图象中正确的是