题目内容
下列有关物质的量的说法中,正确的是( )
| A、O3的摩尔质量为48g/mol |
| B、物质的量的单位是克 |
| C、1mol单质碳在任何条件下的体积都为22.4L |
| D、将2molNaCl晶体加入到1L水中,得到NaCl溶液的浓度就是2mol?L-1 |
考点:摩尔质量,气体摩尔体积
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据摩尔质量数值上等于相对分子质量回答;
B、摩尔是物质的量的单位;
C、摩尔体积与温度和压强、物质的状态有关;
D、阿伏伽德罗常数≈6.02×1023/mol.
B、摩尔是物质的量的单位;
C、摩尔体积与温度和压强、物质的状态有关;
D、阿伏伽德罗常数≈6.02×1023/mol.
解答:
解:A、臭氧中含有3个氧原子,故其相对分子质量为16×3=48,故其摩尔质量为48g/mol,故A正确;
B、物质的量的单位是摩尔,故B错误;
C、只有在标准状况下,1mol气体的体积才为22.4L,故C错误;
D、溶剂的体积不等于溶液的体积,无法计算物质的量浓度,故D错误.
故选A.
B、物质的量的单位是摩尔,故B错误;
C、只有在标准状况下,1mol气体的体积才为22.4L,故C错误;
D、溶剂的体积不等于溶液的体积,无法计算物质的量浓度,故D错误.
故选A.
点评:本题考查物质的量的计算,难度不大,掌握相关概念是正确解答本题的关键.

练习册系列答案
相关题目
汽油燃烧产生的汽车尾气中,所含主要气体污染物之一的是( )
| A、可吸入颗粒物 |
| B、硫的氧化物 |
| C、磷的氧化物 |
| D、碳的氧化物 |
已知反应X+Y═M+N为放热反应,对该反应的下列说法中正确的是( )
| A、X的能量一定高于M |
| B、Y的能量一定高于N |
| C、X和Y的总能量一定高于M和N的总能量 |
| D、X和Y的总能量一定低于M和N的总能量 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下,1mol乙烯共用电子对数为4NA |
| B、1mol乙醛与足量新制Cu(OH)2悬浊液反应,转移电子数目为NA |
| C、标准状况下,1L戊烷充分燃烧后生成气态产物的分子数为5/22.4 NA |
| D、0.1mol乙烯和乙醇的混合物完全燃烧所消耗的氧原子数一定为0.6 NA |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3NA |
| B、1mol H2O2完全分解生成H2O和O2时,转移了NA个电子 |
| C、1mol C10H22分子中,含有共价键数目为32NA |
| D、0.5mol Na2O2中含有NA个阴离子 |
化合物丙由如下反应:C4H10O(甲)
C4H8(乙)
C4H8Br2(丙)得到,丙不可能的是( )
| 浓H2SO4 |
| △ |
| Br2 |
| CCl4 |
| A、CH3CH2CHBrCH2Br |
| B、CH3CH(CH2Br)2 |
| C、CH3CHBrCHBrCH3 |
| D、(CH3)2CBrCH2Br |
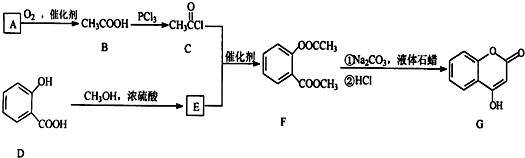
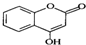 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成