题目内容
右图关于原电池或电解池的叙述中,正确的是( )


| A、e是稀硫酸,c、d是金属Cu,在AB两端接上一个电流表,可看到电流表指针偏转 |
| B、用该装置做Fe片表面电镀Cu的实验,c、d是Fe片和Cu片,e是CuSO4溶液,A、B接直流电源的正负极 |
| C、c、d都用石墨,e为CuCl2溶液,A、B分别连接直流电源正、负极,c极反应式为:2Cl--2e-=Cl2↑ |
| D、c、d分别用Zn和Fe,e是经过酸化的3% NaCl溶液,AB两端接电流表是验证牺牲阳极的阴极保护法实验装置 |
考点:原电池和电解池的工作原理
专题:
分析:A、c、d是金属Cu,两个电极相同,不能构成原电池;
B、镀件是阳极与电源的正极相连;
C、A与正极相连是阳极,c极反应式为:2Cl--2e-=Cl2↑;
D、锌做负极,铁做正极,发生的是锌的吸氧腐蚀;
B、镀件是阳极与电源的正极相连;
C、A与正极相连是阳极,c极反应式为:2Cl--2e-=Cl2↑;
D、锌做负极,铁做正极,发生的是锌的吸氧腐蚀;
解答:
解:A、c、d是金属Cu,两个电极相同,不能构成原电池,故A错误;
B、镀件是阳极与电源的正极相连,所以A、B接直流电源的负正极,故B错误;
C、A与正极相连是阳极,c极反应式为:2Cl--2e-=Cl2↑,故C正确;
D、锌做负极,铁做正极,发生的是锌的吸氧腐蚀,是验证牺牲阳极的阴极保护法的实验装置,故D正确;
故选CD.
B、镀件是阳极与电源的正极相连,所以A、B接直流电源的负正极,故B错误;
C、A与正极相连是阳极,c极反应式为:2Cl--2e-=Cl2↑,故C正确;
D、锌做负极,铁做正极,发生的是锌的吸氧腐蚀,是验证牺牲阳极的阴极保护法的实验装置,故D正确;
故选CD.
点评:本题考查了原电池原理的分析判断,注意电解质溶液不同,电极与电极反应变化,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
下列化学方程式与所述事实相符,且正确的是( )
| A、检验燃尽的火柴头浸泡液中含有氯元素ClO3-+3NO2-+Ag+═AgCl↓+3NO3- |
| B、用淀粉碘化钾溶液和醋酸鉴别真假碘盐:IO3-+5I-+6H+=3I2+3H2O |
| C、用纸层析法分离Fe3+和Cu2+时,最后阶段充分氨熏:Cu2++2NH3?H2O=Cu(OH)2↓+2NH4+ |
| D、在硫酸亚铁溶液中加入等物质的量的硫酸铵,制备摩尔盐FeSO4+(NH4)2SO4+6H2O═(NH4)2SO4?FeSO4?6H2O↓ |
下列有关实验操作不正确的是( )
| A、给盛有液体的烧瓶加热时,需要加碎瓷片或沸石 |
| B、CCl4萃取碘水中碘的实验,分液时,水层应从分液漏斗下口放出,CCl4层从应上口倒出 |
| C、用容量瓶配制溶液,定容时加水超过了刻度线,必须进行重新配制 |
| D、测定溶液pH时,应用干燥洁净的玻璃棒蘸取溶液点在pH试纸上跟标准比色卡对照 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、1 mol N2所含有的原子数为NA |
| B、1 mol?L-1 NaCl溶液中含有的钠离子数目为NA |
| C、标准状况下,22.4 LCO所含的原子数为NA |
| D、24 g O2和24 g O3所含的氧原子数都是1.5NA |
若NA为阿伏伽德罗常数的值,下列说法不正确的是( )
| A、1molCl2与足量的铁反应,转移电子数为3NA |
| B、常温常压下,1mol氦气含有的原子数为NA |
| C、标准状况下,2.24L丁烷分子所含的C-H 键数为NA |
| D、1molNa2O2所含的阴离子数目为NA |
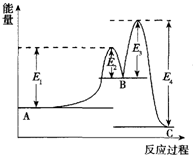 某反应由两步反应A→B→C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
某反应由两步反应A→B→C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )| A、两步反应均为吸热反应 |
| B、加入催化剂会改变反应的焓变 |
| C、三种化合物中C最稳定 |
| D、A→C反应中△H=E1-E2 |
下列有关叙述正确的是( )
| A、明矾在水中生成的Al(OH)3胶体有吸附性,因此常用明矾对水进行净化和消毒 |
| B、二氧化硅具有较强的导电性,可用于制造光导纤维 |
| C、CO2、SO2、NO2都能和碱溶液发生反应,因此它们都属于酸性氧化物 |
| D、常温下干燥的氯气不与铁反应,所以可以用钢瓶贮存液氯 |