题目内容
将一定量的硫化铵固体置于恒容密闭容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH4HS(s)?NH3(g)+H2S(g),下列选项中不能用来判断该反应已达平衡状态的是( )
| A、v正(NH3)=v逆(H2S) |
| B、密闭容器中混合气体的密度不变 |
| C、密闭容器中的压强不变 |
| D、密闭容器中氨气的体积分数不变 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论.
解答:
解:NH4HS(s)?NH3(g)+H2S(g),
A.v正(NH3)=v逆(H2S),且化学反应速率之比等于化学计量数之比,故正逆反应速率相等,故A不选;
B.密度=
,气体的总质量会变,体积不变,故密闭容器中混合气体的密度不变可作为判断是否达到化学平衡状态的依据,故B不选;
C.反应前后气体的体积不等,故密闭容器中的压强不变可作为判断是否达到化学平衡状态的依据,故C不选;
D.NH3与H2S的物质的量之比为1:1,故密闭容器中氨气的体积分数始终为50%,故密闭容器中氨气的体积分数不变不能作为判断是否达到化学平衡状态的依据,故D可选;
故选D.
A.v正(NH3)=v逆(H2S),且化学反应速率之比等于化学计量数之比,故正逆反应速率相等,故A不选;
B.密度=
| 总质量 |
| 体积 |
C.反应前后气体的体积不等,故密闭容器中的压强不变可作为判断是否达到化学平衡状态的依据,故C不选;
D.NH3与H2S的物质的量之比为1:1,故密闭容器中氨气的体积分数始终为50%,故密闭容器中氨气的体积分数不变不能作为判断是否达到化学平衡状态的依据,故D可选;
故选D.
点评:本题考查化学平衡状态的判断,题目难度不大.要注意把握平衡状态的特征.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
把一块镁铝合金投入到1mol/L HCl溶液里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如下图A所示.下列说法中不正确的是( )


| A、若将关系图改为B图时,则a的取值范围为80<a<90 | ||
B、
| ||
| C、若将关系图改为C图时,则a的取值范围为75<a<90 | ||
| D、a的取值范围为0≤a<50 |
下列各组中的两种物质互为同分异构体的是( )
| A、乙烷和乙酸 |
| B、淀粉和纤维素 |
| C、CH3CH2CH2CH3和CH3CH2CH3 |
D、 和CH3CH=CH2 和CH3CH=CH2 |
在NO2与水的反应中( )
| A、氮元素的化合价不会发生变化 |
| B、NO2只是氧化剂 |
| C、NO2只是还原剂 |
| D、NO2既是氧化剂,又是还原剂 |
 有机物环丙叉环丙烷,由于其特殊的电导结构一直受到理论化学家的注意,其结构如图所示.有关它的说法中错误的是( )
有机物环丙叉环丙烷,由于其特殊的电导结构一直受到理论化学家的注意,其结构如图所示.有关它的说法中错误的是( )| A、其二氯代物有4种 |
| B、它不可能是环丙烷的同系物 |
| C、其分子式为C6H8 |
| D、它所有的原子均在同一平面上 |
下列叙述不正确的是( )
| A、金属与盐溶液的反应不一定都是置换反应 |
| B、简单阴离子都只有还原性 |
| C、与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物 |
| D、分子晶体中一定存在范德瓦耳斯力,不一定存在共价键 |
因其分子中碳原子排列类似金刚石故名“金刚烷”,金刚烷分子中有( )
| A、2个-CH3结构 |
| B、4个-CH2-结构 |
C、4个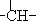 结构 结构 |
D、6个 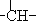 结构 结构 |
下列描述或化学用语书写错误的是( )
| A、向Fe(OH)3胶体中滴加稀硫酸,先生成红褐色沉淀,后沉淀逐渐溶解 |
| B、向铜粉中加入稀硫酸,铜粉不溶解,再加入硝酸钾固体,铜粉逐渐溶解 |
| C、向明矾(KAl(SO4)2?12H2O)溶液中滴入Ba(OH)2溶液,SO42-恰好完全沉淀时的离子方程式为:Ba2++3OH-+Al3++SO42-═BaSO4↓+Al(OH)3↓ |
| D、氯碱工业和金属钠的冶炼都用到了NaCl,阳极上发生的电极反应都是:2Cl-+2e-=Cl2↑ |
