题目内容
下列有关热化学方程式的叙述正确的是
A.已知2H2 (g)+O2(g)═2H2O(g)△H=﹣483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol
B.含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=﹣57.4kJ/mol
C.已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定
D.已知C(s)+O2(g)═CO2(g) △H1;C(s)+1/2 O2(g)═CO(g)△H2,则△H1>△H2
B
【解析】
试题分析:A.由于气态水的能量比液态水高,所以已知2H2 (g)+O2(g)═2H2O(g)△H=﹣483.6kJ/mol,则氢气的燃烧热大于241.8kJ/mol,错误;B.含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,由于20gNaOH的物质的量是0.5mol,所以则表示该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=﹣57.4kJ/mol ,正确;C.物质含有的能量越低,稳定性就越强,由于C(石墨,s)═C(金刚石,s)的反应是吸热反应,所以金刚石的能量高,,则金刚石不如石墨稳定,错误;D.物质越多,反应反应的热量就越大,C(s)+O2(g)═CO2(g) △H1;C(s)+1/2 O2(g)═CO(g)△H2,则△H1<△H2,错误。
考点:考查有关热化学方程式的叙述的正误判断的知识。

(10分)常温常压下,断裂1mol气体分子化学键所吸收的能量或形成1mol气体分子化学键所放出的能量称为键能(单位为kJ.mol-1),根据下表键能数据(kJ·mol-1)回答问题:
化学键 | C-F | C-Cl | C-I | H-H | S=S | H-S |
键能 | 427 | 330 | 218 | 436 | 255 | 339 |
(1)由表中数据预测C-Br键的键能范围:_________<C-Br键能<_________(回答数值和单位)
(2)热化学方程式2H2(g)+S2(g) = 2H2S(g);△H= QkJ·mol-1;则Q=
(3)已知下列热化学方程式:
①O2 (g) = O+2(g) + e- 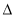 H1= +1175.7 kJ·mol-1 ②PtF6(g) + e- = PtF6—(g)
H1= +1175.7 kJ·mol-1 ②PtF6(g) + e- = PtF6—(g) 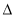 H2= -771.1 kJ·mol-1
H2= -771.1 kJ·mol-1
③O2+PtF6-(s) = O2+(g) + PtF6-(g)  H3= +482.2 kJ·mol-1
H3= +482.2 kJ·mol-1
则反应O2(g) + (g) = O2+PtF6-(s) 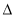 H=_____________ kJ·mol-1。
H=_____________ kJ·mol-1。
 CO2(g)+H2(g),达到平衡后CO2的物质的量为0.6mol,再通入4molH2O(g),当再次达到平衡后,CO2的物质的量可能是
CO2(g)+H2(g),达到平衡后CO2的物质的量为0.6mol,再通入4molH2O(g),当再次达到平衡后,CO2的物质的量可能是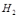 成金属氢化物的材料
成金属氢化物的材料