题目内容
Na2CO3溶液中含有少量的NaHCO3,除杂质的最好方法是( )
| A、加热 |
| B、通入少量的CO2 |
| C、加入适量的NaOH |
| D、加入适量的盐酸 |
考点:物质的分离、提纯的基本方法选择与应用
专题:化学实验基本操作
分析:若Na2CO3溶液中混有少量 NaHCO3溶液,利用NaHCO3能与氢氧化钠反应生成碳酸钠和水而除杂,以此来解答.
解答:
解:A.加热时,沸点不超过100℃,而NaHCO3受热的温度约为150℃,难以分解而除去,故A不选;
B.通入少量的CO2,Na2CO3溶液反应生成NaHCO3,不能用于除杂,故B不选;
C.加NaOH与NaHCO3反应生成Na2CO3,可用于除杂,故C选;
D.二者都与盐酸反应,不能用于除杂,故D错误.
故选C.
B.通入少量的CO2,Na2CO3溶液反应生成NaHCO3,不能用于除杂,故B不选;
C.加NaOH与NaHCO3反应生成Na2CO3,可用于除杂,故C选;
D.二者都与盐酸反应,不能用于除杂,故D错误.
故选C.
点评:本题考查物质的分离、提纯,侧重除杂的考查,把握碳酸钠、碳酸氢钠的性质及差异为解答的关键,注意除杂的原则,易错点为A,题目难度不大.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、在常温常压下,2.8 g N2和CO的混合气体所含电子数为1.4NA | ||
| B、1 molCl2与足量Fe完全反应,转移3NA个电子 | ||
C、1 L 0.1 mol?L-1 NaHCO3溶液中含有0.1 NA个HCO
| ||
| D、7.8g Na2O2中阴离子数为0.2NA |
下列电解质溶液中,离子浓度关系正确的是( )
| A、(NH4)2Fe(SO4)2溶液中:c(SO42-)>c(Fe2+)>c(NH4+)>c(H+)>c(OH-) |
| B、PH相等的①CH3COONa②NaAlO2溶液比较:c(Na+):①<② |
| C、NH4HSO4溶液中:c(H+)>c(OH-)+c(SO42-) |
| D、NaAlO2溶液中通入过量CO2后:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
常温下,现有0.1mol/L的NH4HCO3溶液,pH=7.8.已知含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如图所示.下列说法不正确的是( )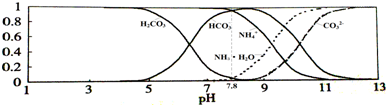

| A、NH4HCO3溶液中存在下列守恒关系:c(NH4+)+c(NH3?H2O)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| B、往该溶液中逐滴滴加氢氧化钠时NH4+和HCO3-浓度逐渐减小 |
| C、通过分析可知常温下Kb(NH3?H2O)>Ka1(H2CO3) |
| D、当溶液的pH=9时,溶液中存在下列关系:c(HCO3-)>c(NH4+)>c(NH3?H2O)>c(CO32-) |
工业炼铁是在高炉中进行的,高炉炼铁的主要反应是:
①2C(焦炭)+O2(空气)
2CO ②Fe2O3+3CO
2Fe+3CO2
该炼铁工艺中,对焦炭的实际使用量要远远高于按照化学方程式计算所需其主要原因是( )
①2C(焦炭)+O2(空气)
| ||
| ||
该炼铁工艺中,对焦炭的实际使用量要远远高于按照化学方程式计算所需其主要原因是( )
| A、CO过量 |
| B、CO与铁矿石接触不充分 |
| C、炼铁高炉的高度不够 |
| D、CO与的反应有一定限度 |
下列物质中,只含离子键的是( )
| A、N2 |
| B、HCl |
| C、MgCl2 |
| D、KOH |
同温同压,相同体积的CO和C2H4具有相同的( )
①分子数 ②原子总数 ③碳原子数 ④质量.
①分子数 ②原子总数 ③碳原子数 ④质量.
| A、①②③④ |
| B、②③④ |
| C、①④ |
| D、①②③ 点燃 |