题目内容
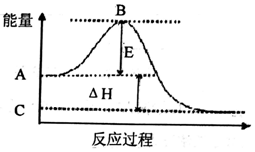
20.下列有关实验说法正确的是( )| A. | 测定中和反应的反应热时,将碱缓慢倒入酸中,所测结果△H偏小 | |
| B. | 检验溶液中是否有SO42-时,应先将溶液用稀硝酸酸化 | |
| C. | 滴定管在装标准溶液前,必须先用待装标准溶液润洗 | |
| D. | NaHCO3溶液和稀盐酸可以用互滴的方法鉴别 |
分析 A.测定中和反应的反应热时,应迅速混合,防止热量散失;
B.用稀硝酸酸化,可将亚硫酸根离子氧化为硫酸根离子,干扰检验;
C.滴定管洗净后需要润洗,否则浓度偏小;
D.NaHCO3溶液和稀盐酸的反应与量无关,混合后立即生成气体.
解答 解:A.测定中和反应的反应热时,应迅速混合,防止热量散失,而将碱缓慢倒入酸中,热量减小,所测结果△H偏大,故A错误;
B.用稀硝酸酸化,可将亚硫酸根离子氧化为硫酸根离子,干扰检验,应先加盐酸,后加氯化钡检验硫酸根离子,故B错误;
C.滴定管洗净后需要润洗,否则浓度偏小,则滴定管在装标准溶液前,必须先用待装标准溶液润洗,故C正确;
D.NaHCO3溶液和稀盐酸的反应与量无关,混合后立即生成气体,则用互滴的方法不能鉴别,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握中和热测定、离子检验、仪器实验及物质鉴别为解答本题的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
10.化学与生产、生活和科研密切相关,下列说法错误的是( )
| A. | 用菜籽油浸泡花椒制得花椒油的过程未发生化学变化 | |
| B. | 河水中有许多杂质和有害细菌,加入明矾消毒杀菌后可以饮用 | |
| C. | 把浸泡过KMnO4溶液的硅藻土放在水果箱里可延长水果的保鲜期 | |
| D. | 对医疗器械高温消毒时,病毒蛋白质受热变性 |
15.已知某离子反应为:8Fe2++NO3-+10H+=NH4++8Fe3++3H2O,下列说法不正确的是( )
| A. | Fe2+为还原剂,NO3-被还原 | |
| B. | 消耗l mol氧化剂,转移电子8 mol | |
| C. | 氧化产物与还原产物的物质的量之比为1:8 | |
| D. | 若把该反应设计为原电池,则负极反应式为 Fe2+-e-=Fe3+ |
5.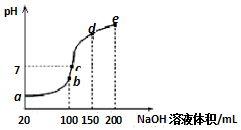 常温下,现向50mL 0.1mol•L-1 NH4HSO4溶液中滴加0.05mol•L-1 NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生).下列说法正确的是( )
常温下,现向50mL 0.1mol•L-1 NH4HSO4溶液中滴加0.05mol•L-1 NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生).下列说法正确的是( )
 常温下,现向50mL 0.1mol•L-1 NH4HSO4溶液中滴加0.05mol•L-1 NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生).下列说法正确的是( )
常温下,现向50mL 0.1mol•L-1 NH4HSO4溶液中滴加0.05mol•L-1 NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生).下列说法正确的是( )| A. | b点溶液中离子浓度由大到小的顺序为:c(Na+)>c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 图中b、c、d、三点溶液中水的电离程度最大的是c点 | |
| C. | b点后滴加NaOH溶液过程中,NH3•H2O的电离程度逐渐减小 | |
| D. | pH=7时,溶液中c(H+)+c(Na+)+c(NH4+)=c(SO42-)+c(OH-) |
3.对于S+2KNO3+3C$\frac{\underline{\;\;△\;\;}}{\;}$K2S+N2↑+3CO2↑下列说法,不正确的是( )
| A. | 该反应中还原剂是C,还原产物有两种 | |
| B. | 若有32g硫参加反应,则被硫氧化的碳单质物质的量为3mol | |
| C. | 若在标准状况下生成8.96L气体,则转移的电子数为1.2NA | |
| D. | 产物中的两种气体在一定条件下都能够和Mg发生反应 |