题目内容
18.盐酸和氨水恰好完全反应后,所得溶液中离子浓度的关系正确的是( )| A. | c(NH4+)>c(Cl-)>c(H+)>c(OH-) | B. | c(NH4+)>c(Cl-)>c(OH-)>c(H+) | ||
| C. | c(Cl-)>c(NH4+)>c(H+)>c(OH-) | D. | c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
分析 盐酸为强电解质,一水合氨为弱电解质,盐酸氨水恰好完全反应生成NH4Cl,为强酸弱碱盐,水解呈酸性,再结合电荷守恒判断c(Cl-)、c(NH4+)浓度大小.
解答 解:盐酸和氨水恰好完全反应生成NH4Cl,为强酸弱碱盐,水解呈酸性,则c(H+)>c(OH-),再结合电荷守恒得c(Cl-)>c(NH4+),因水解程度较小,则c(NH4+)>c(H+),则离子浓度大小关系为c(Cl-)>c(NH4+)>c(H+)>c(OH-),
故选C.
点评 本题以酸碱混合溶液定性判断为载体考查离子浓度大小比较,侧重考查分析能力,注意区别二者呈碱性原因,熟练运用守恒思想解答问题,题目难度中等.

练习册系列答案
相关题目
9.现有一组物质:KCl、Na2SO4、NaCl、NH4Cl,某化学兴趣小组的同学进行了以下实验:
分别取少量上述溶液于4支试管中,然后分别加入Ba(OH)2溶液并加热,用湿润的红色石蕊试纸在试管口检验.上述操作不能鉴别出来的物质是KCl、NaCl.对于可以鉴别的物质,请填写表(可不填满):
分别取少量上述溶液于4支试管中,然后分别加入Ba(OH)2溶液并加热,用湿润的红色石蕊试纸在试管口检验.上述操作不能鉴别出来的物质是KCl、NaCl.对于可以鉴别的物质,请填写表(可不填满):
| 可以鉴别的物质 | 实验现象 | 有关反应的化学方程式 |
| . |
6.下列说法正确的是.
| A. | 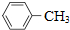 的一溴代物和 的一溴代物和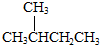 的一溴代物都有4种(不考虑立体异构) 的一溴代物都有4种(不考虑立体异构) | |
| B. | CH3CH=CHCH3分子中的四个碳原子在同一直线上 | |
| C. | 按系统命名法,化合物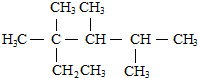 的名称是2,3,4-三甲基-2-乙基戊烷 的名称是2,3,4-三甲基-2-乙基戊烷 | |
| D. | 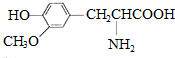 与 与 都是α-氨基酸且互为同系物 都是α-氨基酸且互为同系物 |
13.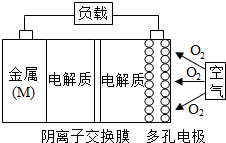 金属(M)-空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH)n,已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )
金属(M)-空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH)n,已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )
 金属(M)-空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH)n,已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )
金属(M)-空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH)n,已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )| A. | 采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面 | |
| B. | 比较Mg,Al,Zn三种金属-空气电池,Al-空气电池的理论比能量最高 | |
| C. | M-空气电池放电过程的正极反应式:4M++nO2+2nH2O+4ne-=4M(OH)n | |
| D. | 在Mg-空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜 |
3.短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,Y是迄今发现的非金属性最强的元素,在周期表中Z位于IA族,W与X属于同一主族.下列说法正确的是( )
| A. | 元素X、W的简单阴离子具有相同的电子层结构 | |
| B. | 由Y、Z两种元素组成的化合物是离子化合物 | |
| C. | W的简单气态氢化物的热稳定性比Y的强 | |
| D. | 原子半径:r(X)<r(Y)<r(Z)<r(W) |
13.NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 14g乙烯与14g苯含有的氢原子数均为2NA | |
| B. | 0.1molFe3+与足量的HI溶液反应,转移的电子数为0.1NA | |
| C. | 1L0.1mol•L-1NaHS溶液中,HS-与H2S数目之和为0.1NA | |
| D. | 6.4g铜溶于30mL10mol•L-1硝酸中,产生气体的分子数为0.2NA |
14.下列离子方程式中,正确的是( )
| A. | 盐酸与氨水混合:H++OH-═H2O | |
| B. | 金属钠投入水中:Na+2H2O═Na++2OH-+H2↑ | |
| C. | 碳酸钠与过量稀盐酸:CO32-+2H+═CO2↑+H2O | |
| D. | 氯气与碘化钾溶液的反应:Cl2+I-=I2+Cl- |
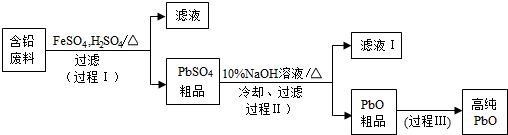
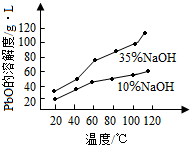
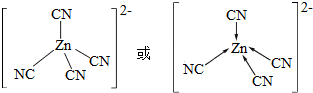 .
.