题目内容
1.下列各项因素中能够对化学反应速度起决定作用的是( )| A. | 温度 | B. | 浓度 | C. | 催化剂 | D. | 物质性质 |
分析 影响化学反应速率的因素有内因和外因,内因为物质的性质,为主要因素,以此解答该题.
解答 解:影响化学反应速率的因素中,反应物的结构与性质是决定性的因素,即最主要因素,而温度、浓度、压强、催化剂等为次要因素.
故选D.
点评 本题考查学生影响化学反应速率的因素,为高频考点,注意反应物的结构与性质是决定性的因素这一点是关键,难度不大.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
11. 如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
 如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )| 选项 | a | b | c |
| A | Fe | FeCl3 | FeCl2 |
| B | HCl | Cl2 | HClO |
| C | H2SO4 | SO2 | SO3 |
| D | CH2=CH2 | CH3CH2OH | CH3CHO |
| A. | A | B. | B | C. | C | D. | D |
12.在标准状况下等物质的量的CO2和NO2不相同的是( )
| A. | 分子数 | B. | 原子数 | C. | 体积 | D. | 质量 |
9. (1)某实验小组为了探究影响化学反应速率的因素,进行了稀硫酸与金属铁反应的对照实验,实验数据如下:
(1)某实验小组为了探究影响化学反应速率的因素,进行了稀硫酸与金属铁反应的对照实验,实验数据如下:
对比实验1和3,表明影响化学反应速率的因素是浓度的大小;此外,该实验表明影响化学反应速率的因素还有固体表面积(说出一种即可).
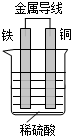
(2)用如图原电池装置可加快铁与稀硫酸反应的速率,此装置可以把化学能转化为电能,其中铁作负极(填“负极”或“正极”).
(3)举出生活中你熟悉的一种电池普通干电池,手机充电电池,铅蓄电池.
 (1)某实验小组为了探究影响化学反应速率的因素,进行了稀硫酸与金属铁反应的对照实验,实验数据如下:
(1)某实验小组为了探究影响化学反应速率的因素,进行了稀硫酸与金属铁反应的对照实验,实验数据如下:| 实验序号 | 金属质量 /g | 金属状态 | c(H2SO4) /mol•L-1 | V(H2SO4) /mL | 反应前溶液温度/℃ | 金属消失的时间/s |
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 50 |
| 3 | 0.10 | 丝 | 1.0 | 50 | 20 | 125 |
| 4 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 |
(2)用如图原电池装置可加快铁与稀硫酸反应的速率,此装置可以把化学能转化为电能,其中铁作负极(填“负极”或“正极”).
(3)举出生活中你熟悉的一种电池普通干电池,手机充电电池,铅蓄电池.
16.下列反应中,属于加成反应的是( )
| A. | CH2=CH2+HCl$→_{△}^{催化剂}$CH3CH2Cl | |
| B. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | |
| C. |  | |
| D. | CH3CH2Br+NaOH$→_{△}^{乙醇}$CH2=CH2↑+NaBr+H2O |
6.在20℃时,某气态烃与氧气混合装入密闭容器中,点燃爆炸后,又恢复到20℃.此时容器内气体的压强为反应前的一半,经NaOH溶液吸收后,容器内几乎真空.此烃的化学式可能是( )
| A. | CH4 | B. | C3H4 | C. | C2H4 | D. | C4H8 |
10.反应N2(g)+3H2(g)?2NH3(g)在密闭容器中进行.下列关于该反应的说法中错误的是( )
| A. | 升高温度能加快反应速率 | |
| B. | 减小压强会减慢反应速宇. | |
| C. | N2和H2能100%转化为NH3 | |
| D. | 反应达到平衡状态时,正、逆反应的速率都为0 |
11.若NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 28g氮气中含有6NA对共用电子对 | |
| B. | 1molH2O2完全分解时转移电子2NA个 | |
| C. | 标况下,3.5g35Cl2所含中子数为0.1NA | |
| D. | 常温、常压下,32gO2和O3混合气体中含有2NA个原子 |