题目内容
现用质量分数为98%、密度为1.84g?cm-3的浓硫酸来配制500mL、0.2mol?L-1的稀硫酸.可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥500mL容量瓶 ⑦托盘天平 ⑧药匙
请完成下列问题:
(1)上述仪器中,在配制稀硫酸时用不到的有 (填序号),需查漏的有 (填序号),查漏的方法: .
(2)经计算,需浓硫酸的体积为 ,现有①10mL ②20mL ③50mL三种规格的量筒,你选用的量筒是 (填序号).
(3)在配制过程中,其它操作都准确,下列能引起所配稀硫酸的浓度偏高的是 操作错误的是 ,(填序号).
①将浓硫酸直接倒入烧杯,再向烧杯中注入蒸馏水稀释浓硫酸
②定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
③转移前,容量瓶中含有少量蒸馏水
④定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
⑤定容时,俯视刻度线.
请完成下列问题:
(1)上述仪器中,在配制稀硫酸时用不到的有
(2)经计算,需浓硫酸的体积为
(3)在配制过程中,其它操作都准确,下列能引起所配稀硫酸的浓度偏高的是
①将浓硫酸直接倒入烧杯,再向烧杯中注入蒸馏水稀释浓硫酸
②定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
③转移前,容量瓶中含有少量蒸馏水
④定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
⑤定容时,俯视刻度线.
考点:溶液的配制
专题:实验题
分析:(1)根据操作步骤选取实验仪器,根据仪器的用途来分析需要查漏的仪器以及查漏的方法;
(2)根据溶液稀释前后溶质的物质的量不变计算所需浓硫酸溶液的体积;根据浓硫酸的体积选取量筒,注意所选量筒的容积应稍大于或等于量取溶液的体积;
(3)根据c=
分析操作对溶质的物质的量或对溶液的体积的影响判断.
(2)根据溶液稀释前后溶质的物质的量不变计算所需浓硫酸溶液的体积;根据浓硫酸的体积选取量筒,注意所选量筒的容积应稍大于或等于量取溶液的体积;
(3)根据c=
| n |
| V |
解答:
解:(1)配制步骤有量取、稀释、移液、洗涤、定容、摇匀等操作,一般用量筒量取浓硫酸溶液在烧杯中稀释,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器有玻璃棒、量筒、胶头滴管、小烧杯、500ml容量瓶,所以用不到的仪器有烧瓶、托盘天平、药匙;需查漏的有容量瓶,查漏的方法:在容量瓶内装入半瓶水,塞紧瓶塞,用右手食指顶住瓶塞,另一只手五指托住容量瓶底,将其倒立(瓶口朝下),观察容量瓶是否漏水.若不漏水,将瓶正立且将瓶塞旋转180°后,再次倒立,检查是否漏水,若两次操作,容量瓶瓶塞周围皆无水漏出,即表明容量瓶不漏水.
故答案为:②⑦⑧; 容量瓶;在容量瓶内装入半瓶水,塞紧瓶塞,用右手食指顶住瓶塞,另一只手五指托住容量瓶底,将其倒立(瓶口朝下),观察容量瓶是否漏水.若不漏水,将瓶正立且将瓶塞旋转180°后,再次倒立,检查是否漏水,若两次操作,容量瓶瓶塞周围皆无水漏出,即表明容量瓶不漏水.
(2)浓硫酸的物质的量浓度为C=
=18.4mol/L;设需要浓硫酸的体积为V,0.2mol/L×0.5L=18.4mol/L×V,V=0.0054L=5.4mL;量筒的容积应稍大于或等于量取溶液的体积,故选①,故答案为:5.4mL;①;
(3)①稀释浓硫酸时,须将浓硫酸注入水中,故①操作错误;
②定容时,加蒸馏水超过刻度线,又用胶头滴管吸出,会导致溶液浓度偏低;
③转移前,容量瓶中含有少量蒸馏水,对所配制溶液浓度无影响;
④定容摇匀后,发现液面低于刻度线是正常的,若又用胶头滴管加蒸馏水至刻度线,则导致溶液浓度偏低;
⑤定容时,俯视刻度线,会导致溶液体积偏小,则溶液浓度偏大;
故能引起所配稀硫酸的浓度偏高的是⑤,操作错误的是①.
故答案为:⑤;①.
故答案为:②⑦⑧; 容量瓶;在容量瓶内装入半瓶水,塞紧瓶塞,用右手食指顶住瓶塞,另一只手五指托住容量瓶底,将其倒立(瓶口朝下),观察容量瓶是否漏水.若不漏水,将瓶正立且将瓶塞旋转180°后,再次倒立,检查是否漏水,若两次操作,容量瓶瓶塞周围皆无水漏出,即表明容量瓶不漏水.
(2)浓硫酸的物质的量浓度为C=
| 103ρw |
| M |
(3)①稀释浓硫酸时,须将浓硫酸注入水中,故①操作错误;
②定容时,加蒸馏水超过刻度线,又用胶头滴管吸出,会导致溶液浓度偏低;
③转移前,容量瓶中含有少量蒸馏水,对所配制溶液浓度无影响;
④定容摇匀后,发现液面低于刻度线是正常的,若又用胶头滴管加蒸馏水至刻度线,则导致溶液浓度偏低;
⑤定容时,俯视刻度线,会导致溶液体积偏小,则溶液浓度偏大;
故能引起所配稀硫酸的浓度偏高的是⑤,操作错误的是①.
故答案为:⑤;①.
点评:本题考查了一定物质的量浓度溶液的配制,难度不大,会根据量取溶液的体积正确选取量筒.

练习册系列答案
相关题目
X、Y为短周期元素,X原子各电子层的电子数之比为1:4:1,它比Y原子多3个电子.下列叙述不正确的是( )
| A、X离子的半径小于Y离子的半径 |
| B、X单质在空气中燃烧不止生成一种物质 |
| C、X、Y形成的化合物为共价化合物 |
| D、Y单质极容易与氢气发生化合 |
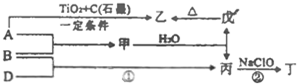 已知:A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol丁分子中不同原子的数目比为1:2,且含有18mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如图所示(某些条件已略去).
已知:A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol丁分子中不同原子的数目比为1:2,且含有18mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如图所示(某些条件已略去).  碳元素在自然界中分布很广,在地壳中其丰富程度位列第14位,远低于氧、硅、铝、铁等元素.但是,碳却是存在形式最复杂的元素,如煤、石油、天然气、动植物体、石灰石、白云石、二氧化碳等.请回答下列问题:
碳元素在自然界中分布很广,在地壳中其丰富程度位列第14位,远低于氧、硅、铝、铁等元素.但是,碳却是存在形式最复杂的元素,如煤、石油、天然气、动植物体、石灰石、白云石、二氧化碳等.请回答下列问题: