题目内容
写出下列反应的化学方程式:
(1)过氧化钠与CO2反应
(2)氯水与硝酸银溶液反应
(3)CO2与次氯酸钙溶液反应
(4)过氧化钠与水反应
(5)Cl2与氢氧化钙溶液反应 .
(1)过氧化钠与CO2反应
(2)氯水与硝酸银溶液反应
(3)CO2与次氯酸钙溶液反应
(4)过氧化钠与水反应
(5)Cl2与氢氧化钙溶液反应
考点:化学方程式的书写,氯、溴、碘及其化合物的综合应用,钠的重要化合物
专题:卤族元素,几种重要的金属及其化合物
分析:(1)过氧化钠和二氧化碳发生氧化还原反应生成碳酸钠和氧气;
(2)氯水中含有盐酸,盐酸和硝酸银发生复分解反应;
(3)二氧化碳与水化合会形成碳酸,碳酸的酸性强于次氯酸;
(4)过氧化钠和水发生氧化还原反应生成氢氧化钠和氧气;
(5)Cl2与氢氧化钙溶液反应生成CaCl2、Ca(ClO)2、H2O.
(2)氯水中含有盐酸,盐酸和硝酸银发生复分解反应;
(3)二氧化碳与水化合会形成碳酸,碳酸的酸性强于次氯酸;
(4)过氧化钠和水发生氧化还原反应生成氢氧化钠和氧气;
(5)Cl2与氢氧化钙溶液反应生成CaCl2、Ca(ClO)2、H2O.
解答:
解:(1)过氧化钠和二氧化碳发生氧化还原反应生成碳酸钠和氧气,反应方程式为:2Na2O2+2CO2=2NaCO3+O2,
故答案为:2Na2O2+2CO2=2NaCO3+O2;
(2)氯水中氯气和水反应:H2O+Cl2?HCl+HClO,稀盐酸和硝酸银反应,生成氯化银和硝酸,HCl+AgNO3═AgCl↓+HNO3
故答案为:H2O+Cl2?HCl+HClO、HCl+AgNO3═AgCl↓+HNO3;
(3)次氯酸钙与水和二氧化碳反应能生成碳酸钙和次氯酸,反应的化学方程式为:Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO,
故答案为:Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO;
(4)过氧化钠和水发生氧化还原反应生成氢氧化钠和氧气,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(5)氯气和氢氧化钙发生氧化还原反应,生成CaCl2、Ca(ClO)2、H2O,该反应为Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O,
故答案为:Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O.
故答案为:2Na2O2+2CO2=2NaCO3+O2;
(2)氯水中氯气和水反应:H2O+Cl2?HCl+HClO,稀盐酸和硝酸银反应,生成氯化银和硝酸,HCl+AgNO3═AgCl↓+HNO3
故答案为:H2O+Cl2?HCl+HClO、HCl+AgNO3═AgCl↓+HNO3;
(3)次氯酸钙与水和二氧化碳反应能生成碳酸钙和次氯酸,反应的化学方程式为:Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO,
故答案为:Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO;
(4)过氧化钠和水发生氧化还原反应生成氢氧化钠和氧气,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(5)氯气和氢氧化钙发生氧化还原反应,生成CaCl2、Ca(ClO)2、H2O,该反应为Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O,
故答案为:Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O.
点评:本题主要考查化学方程式的书写,侧重考查了氯、钠及其化合物的性质及转化,掌握相关物质的化学性质是解题的关键,题目难度不大.

练习册系列答案
相关题目
下列实验操作中错误的是( )
| A、使用试管夹,应从试管底部往上套,夹在试管中上部 |
| B、进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| C、蒸馏时,加热一段时间后发现未加碎瓷片,立刻拨开橡皮塞并投入碎瓷片 |
| D、用稀盐酸清洗做焰色反应的铂丝 |
“物质的量”是联系宏观世界和微观世界的桥梁.下列说法正确的是( )
| A、“摩尔”是“物质的量”的单位 |
| B、1 mol O2的质量是32 g/mol |
| C、任何气体的“气体摩尔体积”均为22.4 L/mol |
| D、10 mL 2 mol/L H2SO4溶液中取出的5 mL溶液,其浓度为1 mol/L |
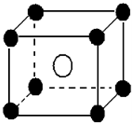 某离子晶体晶胞如图所示,阳离子 X(●)位于立方体的顶点,阴离子Y(○)位于立方体的中心,试分析:
某离子晶体晶胞如图所示,阳离子 X(●)位于立方体的顶点,阴离子Y(○)位于立方体的中心,试分析: